- 257.59 KB
- 2021-02-27 发布
- 1、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 2、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报QQ:3215808601
言程中学2020年秋季高一期中考试
化学试卷
可能用到的相对原子质量:H-1 N-14 O-16 C1--35.5 S-32 Na -23 C-12
第Ⅰ卷
一、选择题(共 15小题,每小题 2 分,共 30分。每小题只有一个选项符合题意)
1、下列说法错误的是( )
A.氯气作水的杀菌消毒剂
B.氯气能使湿润的淀粉碘化钾试纸变蓝,说明Cl2具有氧化性
C.氯气溶于水的离子方程式为Cl2+H2O ==2H++Cl-+ClO-
D.氯气与NaOH溶液反应,Cl2既是氧化剂又是还原剂
2、某地化工厂的贮氯罐意外发生泄漏,下列关于安全处理措施不正确的是( )
A.紧急组织群众沿逆风方向疏散
B.消防队员向贮氯罐周围空气中喷洒稀NaOH溶液
C.处在该环境中的群众,应用浸有稀氨水的毛巾捂住鼻子,趴在低洼处等待救援
D.处在该环境中的群众,应用浸有一定浓度NaHCO3的毛巾捂住鼻子,向高处转移
3、 用等体积的 0.1mol/L 的 BaCl2 溶液,可使相同体积的 Fe2(SO4)3、Na2SO4、KAl(SO4)2三种溶液的完全沉淀,则三种硫酸盐的物质的量浓度之比为( )
A.3:2:1 B.3:1:2 C.2:6:3 D.1:3:2
4.、用 NA 表示阿伏加德罗常数的值,下列叙述中不正确的是( )
A.标况下,22.4 L 氧气的分子数为 NA
B. 1 L0.5 mol/L Na2SO4 溶液中,含有的氧原子总数为 2NA
C.常温常压下,46 g NO2 和 N2O4 的混合气体含有的原子数为 3NA
D. 18 g含有的电子数为 10NA
5、下列关于胶体和溶液的区别的叙述,正确的是( )
A.胶体带电荷,溶液不带电荷
B.向 Fe(OH)3 胶体中逐滴滴入过量的稀硫酸,会先出现红褐色沉淀然后沉淀消失的现象
C.胶体微粒带电荷,溶液中溶质微粒不带电荷
D. 在胶体中通电时,分散质微粒向某一极移动,在溶液中通电时,溶质微粒分别向两极移动
6、如果a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是( )
A. L B. L C. L D. L
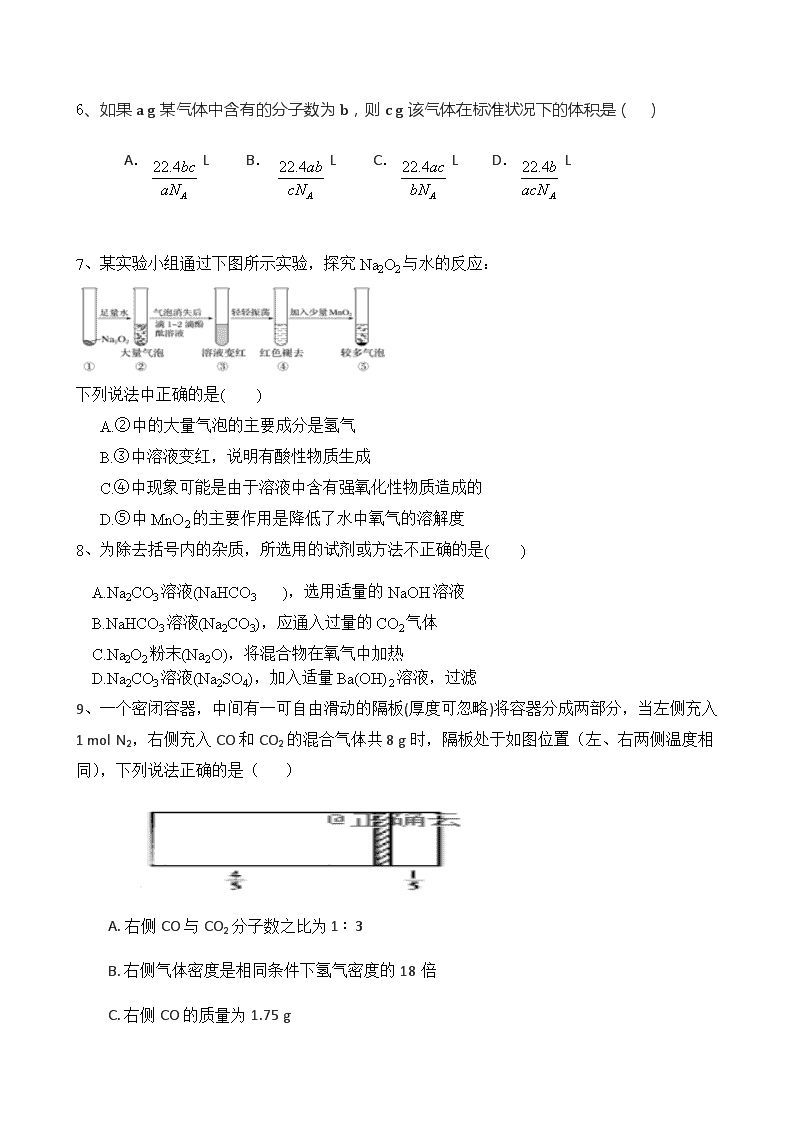
7、某实验小组通过下图所示实验,探究Na2O2与水的反应:
下列说法中正确的是( )
A.②中的大量气泡的主要成分是氢气
B.③中溶液变红,说明有酸性物质生成
C.④中现象可能是由于溶液中含有强氧化性物质造成的
D.⑤中MnO2的主要作用是降低了水中氧气的溶解度
8、为除去括号内的杂质,所选用的试剂或方法不正确的是( )
A.Na2CO3溶液(NaHCO3),选用适量的NaOH溶液
B.NaHCO3溶液(Na2CO3),应通入过量的CO2气体
C.Na2O2粉末(Na2O),将混合物在氧气中加热
D.Na2CO3溶液(Na2SO4),加入适量Ba(OH)2溶液,过滤
9、一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左侧充入1 mol N2,右侧充入CO和CO2的混合气体共8 g时,隔板处于如图位置(左、右两侧温度相同),下列说法正确的是( )
A. 右侧CO与CO2分子数之比为1∶3
B. 右侧气体密度是相同条件下氢气密度的18倍
C. 右侧CO的质量为1.75 g
D. 若隔板处于距离右端1/6处,其他条件不变,则前后两次压强之比为25∶24
10、向100mlNaOH溶液中通入一定量的CO2气体,充分反应后,再向所得溶液中逐滴加入0.2mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如图所示.下列判断正确的是 ( )
A.通入CO2后,所得溶液的溶质成分的物质的量之比为n(NaHCO3):n(Na2CO3)=1:1
B.通入CO2在标准状况下的体积为448mL
C.通入CO2后,所得溶液的溶质成分的物质的量之比为n(NaOH):n(Na2CO3)=1:3
D.原NaOH溶液的浓度为0.2mol/L
11、某溶液中含有HCO、SO、CO、CH3COO-4种阴离子。向其中加入足量的Na2O2固体后,溶液中离子浓度基本保持不变的是(假设溶液体积无变化)( )
A.CH3COO- B.SO
C.CO D.HCO
12、实验室中需要配制2 mol/L的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl质量分别是( )
A. 950 mL,111.2 g B. 500 mL,117 g
C. 1 000 mL,117 g D. 1 000 mL,111.2 g
13、关于钠的描述正确的是( )
①钠在自然界中既有游离态又有化合态 ②金属钠着火可以用泡沫灭火器救火 ③钠的密度比煤油大 ④NaK合金作快中子反应堆的导热剂 ⑤钠比铜活泼,因而钠可以从CuCl2溶液中置换出铜 ⑥钠在空气中燃烧,主要产物为Na2O2
A.①③④⑤⑥ B.③④⑥
C.③④ D.全部
14、某容器真空时,称量其质量为60.4g,此容器充满N2时总质量为66.0g,在相同状况下,充满另一气体时,总质量为74.6g,那么该气体可能是( )
A.Cl2 B.O2 C. SO2 D. HCl
15、能用于工业生产的是
A.钠在氯气中燃烧制氯化钠 B.二氧化锰和浓盐酸共热制氯气
C.氯气与消石灰反应制漂白粉 D.电解NaCl溶液制金属钠
二、选择题(共6小题,每题3分,共18分。每小题1—2个答案)
16、下列各组中两种物质作用时,反应条件或反应物用量改变,对生成物没有影响的是( )
A. Na与O2 B.Ca(OH)2与CO2 C.Na202 与CO2 D. Fe与Cl2
17、下列说法正确的是( )
A.Na2O2遇到湿润的紫色石蕊试纸后,石蕊试纸最终变成蓝色
B.Na2O2与CO2反应生成0.1mol O2时转移电子0.4mol
C.Na2O2投入到CuCl2溶液中有蓝色沉淀及气泡产生
D.向饱和烧碱溶液中加入2g Na2O2,充分反应完后,溶液中Na+的数目不变
18、下列离子方程式的书写及评价均合理的是( )
选项
离子方程式
评价
A
将2mol Cl2通入到含1mol FeI2的溶液中:
2Fe2++2I-+2Cl2=2Fe3++4Cl-+I2
正确; Cl2过量,Fe2+、I-均被氧化
B
将Na2O2固体溶于水:
2Na2O2+2H2O=4Na++4OH-+O2↑
正确; Na2O2是碱性氧化物
C
少量CO2通入到NaClO溶液中:
CO2+H2O+2ClO-=HClO+CO32-
正确;H2CO3的酸性强于HClO
D
Mg(HCO3)2溶液与足量的NaOH溶液反应:
Mg2++2HCO3-+4OH-=Mg(OH)2 ↓+2CO32-+2H2O
正确;Mg(OH)2比MgCO3更难溶
19、下列实验方法能达到实验目的的是( )
A.用紫色石蕊溶液鉴别Cl2和HCl两种气体
B.用淀粉溶液检验溶液中是否存在碘单质
C.用BaCl2溶液鉴别Na2SO4和Na2CO3两种溶液
D.用FeCl2溶液检验新制氯水中含有HClO
20、如图所示装置,正放在桌面上,适用于从 Y口进入的操作是( )
A.瓶内盛一定量的浓硫酸,用于干燥气体
B.X口接量筒,瓶内盛满水,用于测量难溶于水的气体的体积
C.瓶内盛一定量的饱和 NaHCO3 溶液,用于除去 CO2 中混有的杂质气体
D.用排空气法收集O2 , Cl2等气体
21、已知:2Fe2++Br2===2Fe3++2Br-,2Br-+Cl2===Br2+2Cl- , 2Fe3++2I-===2Fe2++I2。向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如下图所示。下列有关说法中,正确的是( )
A.还原性:I-
相关文档
- 山东省日照青山学校2018-2019学年2021-02-27 09:11:427页
- 高考II卷化学试题及答案2021-02-27 09:11:409页
- 人教版初中化学知识点总结(绝对全-2021-02-27 09:11:3923页
- 【化学】河北省保定市2019-2020学2021-02-27 09:11:3716页
- 2019届二轮复习化学能与热能课件(432021-02-27 09:11:3043页
- 2018-2019学年江西省南昌市八一中2021-02-27 09:11:2914页
- 化学卷·2019届黑龙江大庆铁人中学2021-02-27 09:11:286页
- 2021年湖北省中考化学模拟试题含答2021-02-27 09:11:288页
- 苏教版备战高考化学复习必修讲义铝2021-02-27 09:11:284页
- 高考各地化学试题分类汇编和解析2021-02-27 09:11:2616页