- 1.80 MB
- 2021-05-28 发布
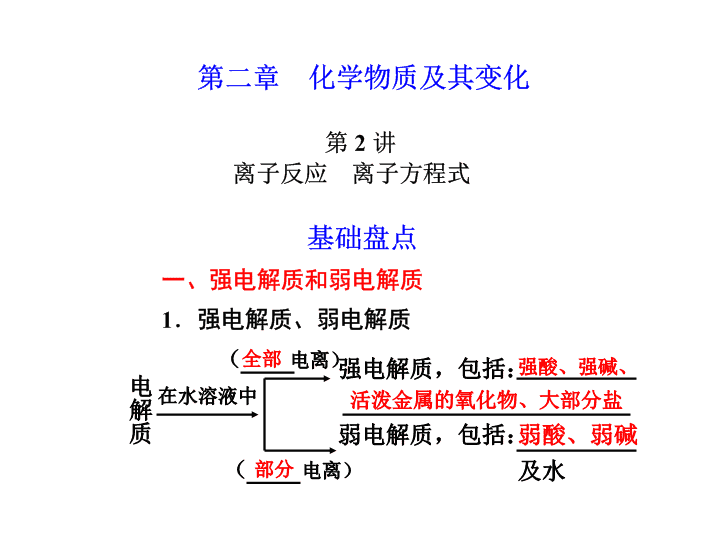
电离)电
解
质在水溶液中
电离)
全部
部分
强电解质,包括:
弱电解质,包括:
强酸、强碱、
活泼金属的氧化物、大部分盐
弱酸、弱碱
及水
(
(
HS-H++S2-
H2SO4===2H++SO 2-4
NaOH===Na++OH- (NH4)2SO4===2NH++SO2-44
H2SH++HS-
==
H++AlO-+H2OAl(OH)3Al3++3OH
-
NaHSO4===Na++H++
SO2-
4
NaHSO4===Na++HSO- 4
2
离子
减小
沉淀 气体 弱电解质
转移
用实际参加反应的离子符号表示离子反
应的式子
一个具体的反应
同一类型的离子反应
原子 电荷
答案 C
×
×
√
√
×
×
√
√
×
×
√
√
×
×
√
√
答案 C
答案 D
答案 B
答案 C
例4 近年高考中10种常考易错离子组合的剖析
注:7、8、9中S2-与不同的金属阳离子反应,其反应原理不同。
答案 D
答案 B
答案 A
解析 离子方程式H++OH-===H2O表示的
是
强酸和强碱中和生成可溶性盐和水的反应。A项中
NH4Cl不是强碱而是盐;B项中Mg(OH)2是难溶于
水
的中强碱;C项中NaHCO3是酸式盐,因此只有D项
符合题意。
D△
答案 B
答案 C
答案 C
答案 D
答案 C
D
答案 C
答案 D
答案 B
褪色 黄色沉淀
还原 氧化
5SO2+2MnO +8H+ 2Mn2++5SO +4H2O
4
2
4
Al3++3OH- Al(OH)3
+2H2O
2
Al(OH)3+OH- AlO
2
2
2Al+2OH— 2AlO +H2
2
2
2Fe2++Cl2 2Fe3++2Cl-
2Fe2++2I-+2Cl2 2Fe3++4Cl-+I2
Ba2++SO BaSO4
NH +OH-
NH3·H2O
Fe3++3H2O Fe(OH)3 +3H+
2
4
4
相关文档
- 部编版小学二年级下册语文教学课件2021-05-28 18:18:2033页
- 外研版英语七年级下册Module 8 Uni2021-05-28 18:17:5350页
- 六年级下册语文教学课件PPT-31成长2021-05-28 18:17:5216页
- 人教部编版语文四年级下册教学课件2021-05-28 18:17:305页
- 人教版一年级数学下册第六单元1002021-05-28 18:16:4912页
- 冀教版一年级数学上册第八单元20以2021-05-28 18:16:496页
- 人教版PEP小学三年级下册英语教学2021-05-28 18:16:3610页
- 人教版小学二年级上册数学教学课件2021-05-28 18:16:2134页
- 部编人教版语文 四年级下册教学课2021-05-28 18:16:1922页
- 北师大版小学一年级下册教学课件-2021-05-28 18:10:109页