- 1.71 MB
- 2021-05-27 发布
水电离产生
的H+或OH
-
弱电解质
水的电离平衡
增大
第十章 水溶液中的离子平衡
可逆
中和
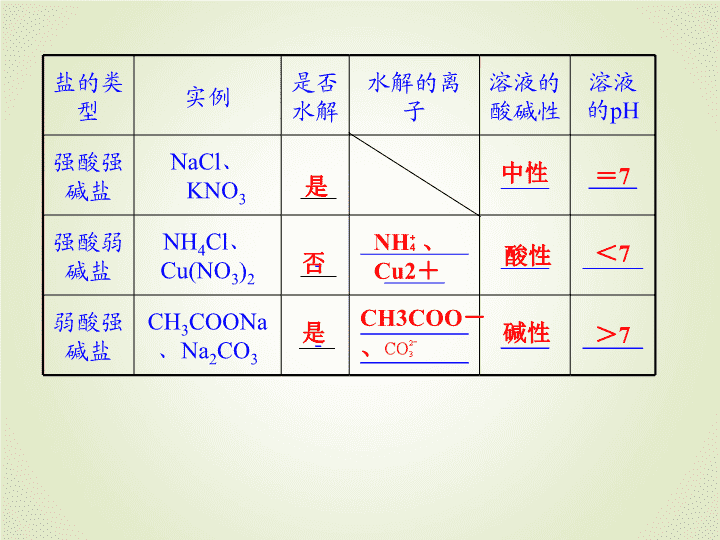
盐的类
型 实例 是否
水解
水解的离
子
溶液的
酸碱性
溶液
的pH
强酸强
碱盐
NaCl、
KNO3 ____ ____
强酸弱
碱盐
NH4Cl、
Cu(NO3)2
_________
_____ ____ _____
弱酸强
碱盐
CH3COONa、
Na2CO3
_________
_________ ____ _____
NH 、
Cu2+
CH3COO-
、CO2
3
中性
酸性
碱性
=7
<7
>7
+
4
是
否
是
弱酸(或弱碱)+OH-(或H+)
NH +H2O
NH3·H2O+H+
+
4
CO +H2O HCO +OH-
Fe3++3H2O Fe(OH)3+3H
+
Al3++3HCO ===Al(OH)3↓+3CO2↑
2-
3
-
3
3
-
越大 越强
右移
右移
右移
增大 增大
增大
增大 减小
减小
增大
减小
减小
减小
答案 C
答案 B
答案 A
答案 C
√
×
解析 显酸性的溶液可能是酸溶液,也可能
是强酸弱碱盐溶液,还可能是酸式盐溶液,如
NaHSO4、NaH2PO4溶液显酸性。
√
解析 0.1 mol/L HA溶液的pH=3,说明HA
为弱酸,则NaA溶液中存在A-的水解平衡。
(4)在滴有酚酞溶液的氨水里,加入NH4Cl至溶
液恰好无色,则此时溶液的pH<7( )
(2010·全国Ⅰ-9B)
×
解析 酚酞的变色范围为8.2~10.0,当溶液
恰好无色时,溶液pH刚刚小于8.2,即可显示无色。
√
解析 酸性CH3COOH>H2CO3>HCO ,CO 的
水解程度比CH3COO-的大。
-3
2-
3
解析 A、D项是电离方程式,B项是CO2溶于
水后的电离过程,C项正确。
C
答案 D
答案 D
答案 A
答案 D
答案 A
答案 B
答案 B
解析 酸性:H2CO3>H2SiO3,根据水解规
律:
Na2SiO3水解程度大于Na2CO3,B项正确。
B
答案 A
BD
A
CO2
3
3HCO
A
TiCl4+xH2O
===TiO2·xH2O+4Cl-
相关文档
- 九年级数学上册第六章反比例函数12021-05-27 19:56:5721页
- 外研版英语八年级下册Module 5 Uni2021-05-27 19:56:3941页
- 三年级数学上册第4单元位置与变换2021-05-27 19:54:5423页
- 部编人教版七年级下册语文教学课件2021-05-27 19:50:5714页
- 人教版小学二年级上册数学教学课件2021-05-27 19:46:1810页
- 西师大版数学二年级下册教学课件-2021-05-27 19:45:2811页
- 二年级数学下册教学课件-2整理和复2021-05-27 19:44:5613页
- 小学三年级作文教学课件新粗心的小2021-05-27 19:39:5825页
- 人教版小学二年级上册数学教学课件2021-05-27 19:39:5813页
- 人教部编版小学二年级语文下册课堂2021-05-27 19:38:0727页