- 98.00 KB
- 2021-04-26 发布
1
《实验活动 8 粗盐中难溶性杂质的去除》教材习题解答
【教材 P88 问题与交流】
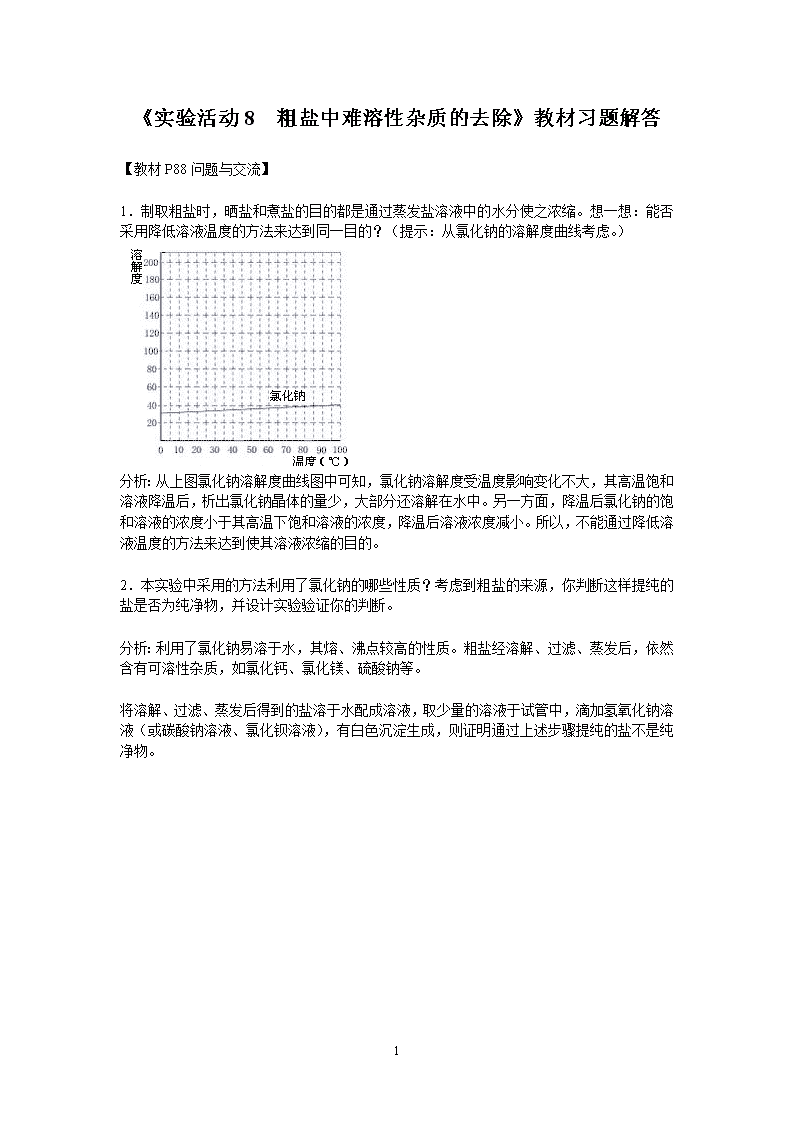
1.制取粗盐时,晒盐和煮盐的目的都是通过蒸发盐溶液中的水分使之浓缩。想一想:能否
采用降低溶液温度的方法来达到同一目的?(提示:从氯化钠的溶解度曲线考虑。)
分析:从上图氯化钠溶解度曲线图中可知,氯化钠溶解度受温度影响变化不大,其高温饱和
溶液降温后,析出氯化钠晶体的量少,大部分还溶解在水中。另一方面,降温后氯化钠的饱
和溶液的浓度小于其高温下饱和溶液的浓度,降温后溶液浓度减小。所以,不能通过降低溶
液温度的方法来达到使其溶液浓缩的目的。
2.本实验中采用的方法利用了氯化钠的哪些性质?考虑到粗盐的来源,你判断这样提纯的
盐是否为纯净物,并设计实验验证你的判断。
分析:利用了氯化钠易溶于水,其熔、沸点较高的性质。粗盐经溶解、过滤、蒸发后,依然
含有可溶性杂质,如氯化钙、氯化镁、硫酸钠等。
将溶解、过滤、蒸发后得到的盐溶于水配成溶液,取少量的溶液于试管中,滴加氢氧化钠溶
液(或碳酸钠溶液、氯化钡溶液),有白色沉淀生成,则证明通过上述步骤提纯的盐不是纯
净物。