- 1.69 MB
- 2021-04-22 发布
元素推断及其综合应用
规范审题与答题
第二轮复习
-
2
-
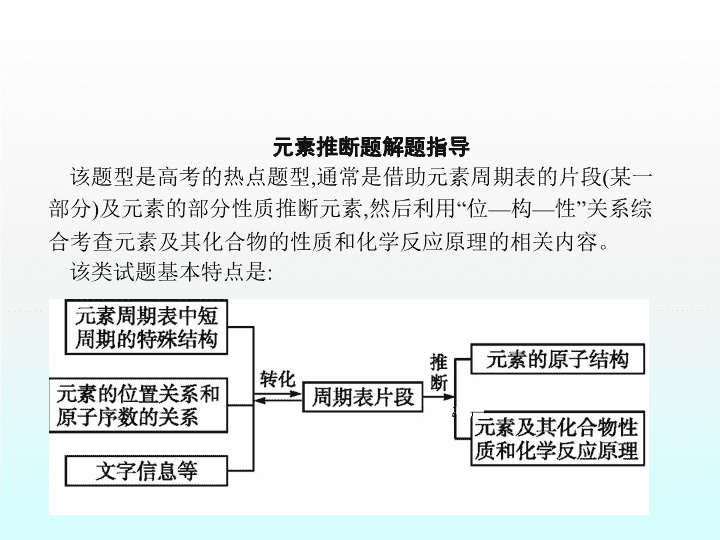
元素推断题解题指导
该题型是高考的热点题型
,
通常是借助元素周期表的片段
(
某一部分
)
及元素的部分性质推断元素
,
然后利用
“
位
—
构
—
性
”
关系综合考查元素及其化合物的性质和化学反应原理的相关内容。
该类试题基本特点是
:
-
3
-
即在实际考查中只呈现元素周期表的某一部分
,
根据呈现的部分结构中提供的信息推断元素
,
推出元素在周期表中的位置
,
就可以快速确定元素的名称、原子结构及相关性质。
-
4
-
根据原子结构、元素周期表的结构及已知条件
,
可推算原子序数
,
判断元素在周期表中的位置等
,
基本思路如下
:
-
5
-
典例
下表给出了五种元素的相关信息
,
其中
A
、
B
、
C
、
D
为短周期元素。
-
6
-
根据上述信息填空
:
(1)E
在元素周期表中的位置是
,
画出
D
的原子结构示意图
:
。
(2)C
与
A
形成的某一化合物能和
C
与
B
形成的另一无色化合物
(
这两种化合物分子中原子个数比皆为
1
∶
2)
一起用作火箭助推剂
,
写出两者发生反应生成无毒物质的化学方程式
:
。
(3)
这五种元素能组成一种用途极广的复盐
(
含一种阴离子和多种阳离子
),
该物质中的
A
、
B
、
C
、
D
、
E
的质量比为
5
∶
56
∶
7
∶
16
∶
14
。写出该化合物的化学式
:
。
解析
:
A
的单质气体可作为清洁能源
,
故
A
为
H;
空气中的主要成分为
O
2
、
N
2
,
而
O
3
号称
“
地球卫士
”,
故
B
为
O;
植物生长的三要素是
N
、
P
、
K,
其中
N
有多种氧化物
,
其中无色
NO
遇空气变为红棕色
NO
2
,
故
C
为
N;
根据单质颜色及燃烧的火焰颜色可知
D
为
S;
根据
E
单质的用途可推知
E
为
Fe
。
(1)Fe
位于元素周期表中第四周期第
Ⅷ
族。
D
为
16
号元素
S,
其原子结构示意图为
。
(2)
根据有关反应物和生成物的信息提示可知该反应是
N
2
H
4
与
N
2
O
4
反应生成
N
2
和
H
2
O
。
(3)
由该复盐中
H
、
O
、
N
、
S
、
Fe
的质量比可计算出其物质的量之比为
20
∶
14
∶
2
∶
2
∶
1,
结合这些元素常见的原子团组合形式可知其化学式为
(NH
4
)
2
Fe(SO
4
)
2
·6H
2
O
。
答案
:
(1)
第四周期第
Ⅷ
族
(2)2N
2
H
4
+N
2
O
4
3N
2
+4H
2
O
(3)(NH
4
)
2
Fe(SO
4
)
2
·6H
2
O
-
9
-
归纳总结
常见元素及其化合物的特性
1
.
形成化合物种类最多的元素、某种单质是自然界中硬度最大的物质的元素或气态氢化物中氢的质量分数最高的元素
:C
。
2
.
空气中含量最多的元素或气态氢化物的水溶液呈碱性的元素
:N
。
3
.
地壳中含量最多的元素、氢化物在通常情况下呈液态的元素
:O
。
4
.
地壳中含量居第二位的元素
:Si
。
5
.
地壳中含量最多的金属元素、最高价氧化物及其水化物既能与强酸反应
,
又能与强碱反应的元素
:Al
。
6
.
元素的气态氢化物和它的最高价氧化物的水化物能发生化合反应的元素
:N
。
-
10
-
7
.
元素的单质在常温下能与水反应放出气体的短周期元素
:Li
、
F
、
Na
。
8
.
单质气体密度最小的元素
:H
。
9
.
一些元素的应用
:Li
、
H
常用于高能电池
,Si
是制造光电池、半导体的常用材料。
10
.Al
是应用最广泛的短周期金属元素
;
14
C
常用于文物年代的鉴定。
-
11
-
1
、
有一应用前景广阔的纳米材料甲
,
甲由
A
、
B
两种短周期非金属元素组成
,
难溶于水
,
且硬度大
,
熔点高。取材料甲与熔融的烧碱反应
,
生成一种含
A
元素的含氧酸盐乙和一种含
B
元素的气体丙
,
且丙能使湿润的红色石蕊试纸变蓝
;
乙能溶于水
,
加盐酸产生白色沉淀
,
盐酸过量沉淀不溶。
(1)
甲的化学式为
(2)
乙的水溶液俗称
,
其可以用来作
(
写出一种用途
)
。
-
12
-
(3)B
元素的一种氢化物丁
,
相对分子质量为
32,
常温下为液体
,
其燃烧放热多且燃烧产物对环境无污染
,
因此可用作火箭燃料、燃料电池燃料等。
①
丁的电子式为
;
②
常温下
,8 g
丁完全燃烧
(
产物均为稳定状态
)
放出的热量为
Q
kJ,
写出其燃烧的热化学方程式
:
;
③
丁与空气可组成碱性燃料电池
,
丁转化为一种稳定的气体和液体
,
写出该电池负极的电极反应式
:
。
-
13
-
答案
:
(1)Si
3
N
4
(2)
水玻璃
(
或泡花碱
)
黏合剂、木材等的防腐剂或防火剂
(
任答一种
)
-
14
-
解析
:
(1)
甲由
A
、
B
两种短周期非金属元素组成
,
难溶于水
,
且硬度大
,
熔点高。甲与熔融烧碱反应
,
生成一种含
A
元素的含氧酸盐乙和一种含
B
元素的气体丙
,
且丙能使湿润的红色石蕊试纸变蓝
,
则甲为
Si
3
N
4
,
乙为
Na
2
SiO
3
,
丙为
NH
3
,
从而推知
,A
为
Si,B
为
N
。
(2)Na
2
SiO
3
的水溶液俗称水玻璃或泡花碱
,
可用作黏合剂、防腐剂、防火剂等。
(3)
①
丁是
B(N)
的一种氢化物
,
相对分子质量为
32,
常温下为液体
,
则丁为
N
2
H
4
,
其电子式为
。
②
8 g N
2
H
4
的物质的量为
0.25 mol,
完全燃烧放出的热量为
Q
kJ,
则
1 mol N
2
H
4
完全燃烧放出的热量为
4
Q
kJ,
热化学方程式为
N
2
H
4
(l)+O
2
(g)==N
2
(g)+2H
2
O(l)
Δ
H
=-4
Q
kJ·mol
-1
。
③
N
2
H
4
与空气组成碱性燃料电池
,N
2
H
4
转化为一种稳定的气体
(N
2
)
和液体
(H
2
O),N
2
H
4
在负极失去电子发生氧化反应
,
电极反应式为
N
2
H
4
+4OH
-
-4e
-
==N
2
↑+4H
2
O
。