- 98.00 KB
- 2021-04-13 发布
- 1、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 2、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报QQ:3215808601
2012中考化学专题突破—涉及酸碱盐的推断(2012.05)
一、叙述型
1、两种溶液混合,生成了一种沉淀。用酸碱盐的知识回答下列问题。
(1) 若两种溶液均为无色,生成的白色沉淀不溶于稀硝酸,则两种溶液中的溶质可能是 ;
(2) 若两种溶液均为无色,生成的白色沉淀溶于稀硝酸且有气体产生,则两种溶液中的溶质可能是 ;
(3)若一种溶液有色,另一种无色,生成的沉淀溶于稀盐酸且无气体产生,沉淀可能是 。
2、有一种固体混合物,可能由CaCO3、KMnO4、BaCl2、KCl、Na2CO3中的一种或几种物质组成。现取该混合物进行如下实验:(1)将固体混合物投入水中,搅拌后完全溶解,得到无色溶液;(2)往此溶液中滴加盐酸,产生一种能使澄清石灰水变浑浊的无色无味的气体。由上述实验现象可知:该固体混合物中一定存在的是 ,一定不存在的是 ,不能确定的是 。
3、有一包粉末,可能含有碳酸钙、硫酸铜、碳酸钠、硫酸钠、氯化钡中的一种或几种。以下是某同学进行实验并观察到的现象:取少量粉末放入试管中,加水、振荡、静置后,试管中有白色沉淀和无色溶液;再向试管中滴入足量的稀硝酸后,白色沉淀有部分溶解。由此推断,该包粉末的可能组成是:
(1) ;(2) ;(3) 。
4、有一包固体粉末,可能由碳酸钙、硫酸钾、硝酸钠、氯化铁、氯化钡中的一种或几种组成,做实验得到以下结论:
(1)将此固体粉末加到水中,得到白色沉淀,上层溶液为无色。
(2)该白色沉淀部分溶于稀硝酸,且有气体放出。
从实验可判断出,该粉末中一定含有 ,一定不含有 。
5、有一包粉末,可能由NaCl、Na2CO3、FeCl3、Na2SO4中的一种或几种组成,依次进行如下实验:
(1)白色粉末溶于水,得无色透明溶液,加入足量BaCl2溶液生成白色沉淀;
(2)过滤后,向所得沉淀中加入盐酸,沉淀不溶解;
(3)向滤液中加入AgNO3溶液,产生白色沉淀,再加入足量稀硝酸,沉淀不溶解。以上实验,不能确定混合物中是否含有 ,若要检验不能确定的物质是否存在,则上述实验的操作(1)中应加入的试剂是 。
6、现有以下三组物质:(1)Fe(过量)、Cu(OH)2、H2SO4 (2)Zn、AgNO3(过量)、Cu(NO3)2
(3)Fe(过量)、Cu(NO3)2、AgNO3
在各种物质里加水搅拌,待充分反应后,过滤,滤纸上有一种金属的是 ;
有两种金属的是 ;有三种金属的是 ;(填序号)
7、A、B、C、D、E五瓶无色透明溶液,分别是HCl溶液、Na2CO3溶液、MgCl2溶
液、NaNO3溶液、NaOH溶液中的一种。分别进行下列实验:
Ⅰ.将A分别滴入B、C、D、E中,均没有明显现象。
Ⅱ.将B分别滴入A、C、D、E中,C、E中均产生白色沉淀,其余没有明显现象。
Ⅲ.将C分别滴入A、B、D、E中,B中产生白色沉淀,D中有气泡冒出,其余没有明显现象。
(1)A是____________,B是____________,C是____________;
(2)B加入E中的化学方程式是____________ ;
(3)C加入D中的化学方程式是____________ 。
8、有一包白色固体,可能是氯化钙和碳酸钠的混合物,也可能只含有一种物质,为了鉴别它,做了如下实验:
(a)取一些样品溶解在水里,有白色沉淀生成,把悬浊液过滤,得无色滤液.
(b)在滤出的沉淀里加盐酸,有大量气泡产生.
(c)在滤液里加过量硝酸银,有白色沉淀生成,再加入稀硝酸,沉淀部分溶解.
根据上述实验现象判断:
①该白色固体一定含有 _________ .
②操作(a)里滤出的白色沉淀是 _________ ,操作(c)里的白色沉淀是 _________ .
③操作(a)滤液中含有的溶质离子是 _________ .
9、某校初中化学课外小组学生,将一些可溶性化合物溶于水,配制成的甲、乙两瓶溶液,共有H+、K+、Ag+、Ba2+、OH﹣、Cl﹣、NO3﹣、CO32﹣八种离子,每种溶液里含有的四种离子各不相同,已知向甲瓶溶液里滴入紫色石蕊试液后,溶液变成蓝色,据此推知乙瓶溶液中的离子应该是 .
10、甲、乙两个相邻的化工厂,排放的污水经处理后,仍然各溶有以下8种离子(Ag+、Ba2+、Fe3+、Na+、CL﹣、SO42‑、、NO3﹣、OH﹣)中各不相同的4种,若单独排放将造成环境污染.如果将甲、乙两厂的污水,按适当比例充分混合,经沉淀后,排放出的污水转变为无色澄清的硝酸钠溶液,污染程度大为降低,又经测定甲厂污水的pH大于7.试推断:
(1)甲厂污水含有的4种离子是.
(2)乙厂污水含有4种离子是.
11、 某化工厂排放的污水中,常溶有某些对人体有害的物质。初步认为可能含有Fe3+、Ba2+、Na+、OH-、CI-、CO32-、SO42-;为了进一步确认,进行实验检测:
(1)取污水仔细观察,呈无色、透明、均一状态。
(2)向取样的污水中滴入稀硫酸有大量白色沉淀产生,再加稀硝酸白色沉淀不消失。
(3)用pH试纸测定污水的pH值,试纸显深蓝色。
由此可知,该污水中,肯定含有离子是 ,肯定没有的离子是 ,
可能含有的离子是 。
12、A、B、C、D、E五瓶无色透明溶液,分别是HCl溶液、Na2CO3溶液、MgCl2溶
液、NaNO3溶液、NaOH溶液中的一种。分别进行下列实验:
Ⅰ.将A分别滴入B、C、D、E中,均没有明显现象。
Ⅱ.将B分别滴入A、C、D、E中,C、E中均产生白色沉淀,其余没有明显现象。
Ⅲ.将C分别滴入A、B、D、E中,B中产生白色沉淀,D中有气泡冒出,其余没有明显现象。
(1)A是____________,B是____________,C是____________;
(2)B加入E中的化学方程式是____________ ;
(3)C加入D中的化学方程式是____________ 。
二、反应式型
13、已知A、B、C、D、E、F6种物质的转化关系如下:
(1)A+B→C+H2O (2)C+KOH→D↓(蓝色)+E
(3)B+D→C+H2O (4)E+BaCl2→F↓(白色,不溶于稀硝酸)+KCl
根据上述变化关系,推断有关物质的化学式:
A ;B ;C ;D ;E ;F 。
14、有属于酸、碱、盐的5种常见物质A、B、C、D、E,它们之间可以发生如下反应:
(1)A+B→C+H2O (2)C+H2SO4→D↓+A (3)E+AgNO3→AgCl↓+C
根据上述反应,推断下列各物质的化学式:
A ;B ;C ;D ;E 。
三、表格型
15、有失去标签的硝酸钾、碳酸钠、硝酸银、硝酸钙和稀盐酸五瓶溶液。将其任意编号:A、B、C、D、E,进行两两混合,其现象如下表:
实 验
A+B
A+E
B+C
B+E
现 象
产生沉淀
产生沉淀
产生沉淀
产生气泡
(1)试推断并写出五种溶液中溶质的化学式。
A ,B ,C ,D ,E 。
(2)写出有关反应的化学方程式。
A+E B+E
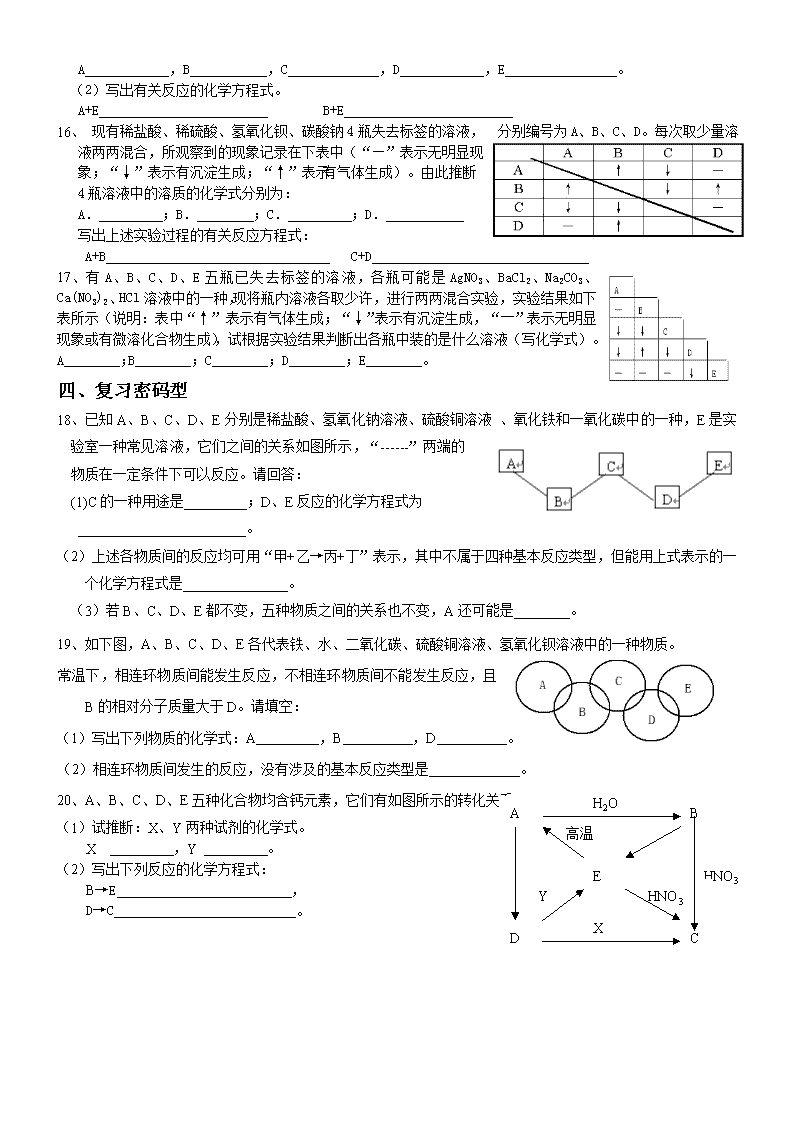
16、 现有稀盐酸、稀硫酸、氢氧化钡、碳酸钠4瓶失去标签的溶液, 分别编号为A、B、C、D。每次取少量溶液两两混合,所观察到的现象记录在下表中(“—”表示无明显现象;“↓”表示有沉淀生成;“↑”表示有气体生成)。由此推断4瓶溶液中的溶质的化学式分别为:
A. ;B. ;C. ;D.
写出上述实验过程的有关反应方程式:
A+B C+D
17、有A、B、C、D、E五瓶已失去标签的溶液,各瓶可能是AgNO3、BaCl2、Na2CO3、Ca(NO3)2、HCl溶液中的一种,现将瓶内溶液各取少许,进行两两混合实验,实验结果如下表所示(说明:表中“↑”表示有气体生成;“↓”表示有沉淀生成,“―”表示无明显现象或有微溶化合物生成),试根据实验结果判断出各瓶中装的是什么溶液(写化学式)。 A________;B________;C________;D________;E________。
四、复习密码型
18、已知A、B、C、D、E分别是稀盐酸、氢氧化钠溶液、硫酸铜溶液 、氧化铁和一氧化碳中的一种,E是实验室一种常见溶液,它们之间的关系如图所示,“------”两端的物质在一定条件下可以反应。请回答:
(1)C的一种用途是_________;D、E反应的化学方程式为
________________________。
(2)上述各物质间的反应均可用“甲+乙→丙+丁”表示,其中不属于四种基本反应类型,但能用上式表示的一个化学方程式是_______________。
(3)若B、C、D、E都不变,五种物质之间的关系也不变,A还可能是________。
19、如下图,A、B、C、D、E各代表铁、水、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质。
常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的相对分子质量大于D。请填空:
(1)写出下列物质的化学式:A ,B ,D 。(2)相连环物质间发生的反应,没有涉及的基本反应类型是_____________。
H2O
HNO3
X
Y
HNO3
高温
A
D
B
C
E
20、A、B、C、D、E五种化合物均含钙元素,它们有如图所示的转化关系:
(1)试推断:X、Y两种试剂的化学式。
X ,Y 。
(2)写出下列反应的化学方程式:
B→E ,
D→C 。
1、(1)AgNO3和NaCl(或Ba(NO3)2和Na2SO4等)
(2)BaCl2和Na2CO3(Ca(OH)2和Na2CO3等)
(3)Cu(OH)2或Fe(OH)2或Fe(OH)3 注:其它合理答案均给分,写名称或名称符号混写也可。
2、CaCO3和KMnO4 、BaCl2;Na2CO3; KCl
3、这包粉末的可能组成是:(1);(2);(3)
4、原固体粉末中一定含有碳酸钙、硫酸钾和氯化钡,一定不含有氯化铁,可能含有硝酸钠。
5、不能确定混合物中是否含有:NaCl,操作(1)中应加入的试剂是Ba(NO3)2
6、(2) (1) (3)
7、(1)A是NaNO3溶液,B是MgCl2溶液,C是Na2CO3溶液;
(2) MgCl2+NaOH==2NaCl+Mg(OH)2↓;
(3)Na2CO3+2HCl==2NaCl+ H2O+ CO2↑。
8、①该白色固体一定含有 氯化钙、碳酸钠 .
②操作(a)里滤出的白色沉淀是 碳酸钙 ,操作(c)里的白色沉淀是 氯化银、碳酸银 .
③操作(a)滤液中含有的溶质离子是 Na+、Cl﹣、CO32﹣
9、 H+、Ag+、NO3﹣、Ba2+
10、(1) Na+、Cl﹣、OH﹣、SO42﹣ (2) Ag+、Ba2+、Fe3+、NO3﹣
11、污水中肯定含有离子是Ba2+、OH-,肯定没有的离子是Fe3+、CO32-、SO42-,
可能含有的离子是Na+、CI-。
12、(1)A是NaNO3溶液,B是MgCl2溶液,C是Na2CO3溶液;
(2) MgCl2+NaOH==2NaCl+Mg(OH)2↓;
(3)Na2CO3+2HCl==2NaCl+ H2O+ CO2↑。
13、A CuO;B HCl;C CuCl2;D Cu(OH)2;E KCl;F BaSO4。
14、A—HNO3 B—Ba(OH)2 C—Ba(NO3)2 D-- BaSO4 E-- BaCl2
15、A-AgNO3 B- Na2CO3 C-Ca(NO3)2 D-KNO3 E-HCl (2)方程式略
16、2SO4 B-- Na2CO3 C-- Ba(OH)2 D—HCl 方程式略
17、 BaCl2 B:HCl C AgNO3 D Na2CO3 E Ca(NO3)2
(1)除铁锈 2NaOH+Cu SO4 = Na2SO4+Cu(OH)2 ↓
(2) 3CO+FeO3高温
2Fe+3CO2 (3)C(或H2)
18、A:Fe B:CuSO4 D:CO2 (2)分解反应
19、A:Fe B:CuSO4 D:CO2 (2)分解反应
20、)AgNO3 CaCl2;(2)Ca(OH)2+CO2===CaCO3↓+H2O CaCl2+2AgNO3===2AgCl↓+Ca(NO3)2
相关文档
- 专题10识记作家作品及文学常识(易错2021-04-13 15:00:586页
- 2020年江苏省苏州市吴江开发区实验2021-04-13 15:00:5229页
- 局党组脱贫攻坚专项巡视“回头看”2021-04-13 15:00:0612页
- 甘肃省兰州市中考化学真题2021-04-13 15:00:0311页
- 圆2016中考专题全国2021-04-13 15:00:029页
- 中考卷 英语专题06 八年级上册 Uni2021-04-13 15:00:0118页
- 初三中考总复习考点复习篇之世界现2021-04-13 15:00:007页
- 2020年某区委常委全体会议上的讲话2021-04-13 14:59:5818页
- 2019年湖南省常德市中考数学试卷2021-04-13 14:59:3827页
- 内蒙古包头市2020中考道德与法治一2021-04-13 14:59:3342页