- 82.00 KB
- 2023-11-23 发布
铝的重要化合物
学习目标
1.掌握“铝三角”及其之间的相互转化
2.有关Al (OH)3沉淀的图像分析及计算
重点
“铝三角”及其之间的相互转化
难点
有关Al(OH)3沉淀的图像分析及计算
学法指导
熟记方程式,理解图像,进而掌握解题规律技巧
自
学
引
导
︵
学
生
课
前
必
须
完
成
︶
一、自主学习:(请同学们认真揣摩练习册 页,你一定能完成下列问题)
完成下列变化的化学方程式: 铝三角及其之间的相互转化
已知:H++AlO2―+H2OAl(OH)3 Al3++3OH―
酸式电离 碱式电离
3
独
立
思
考
合
作
探
究
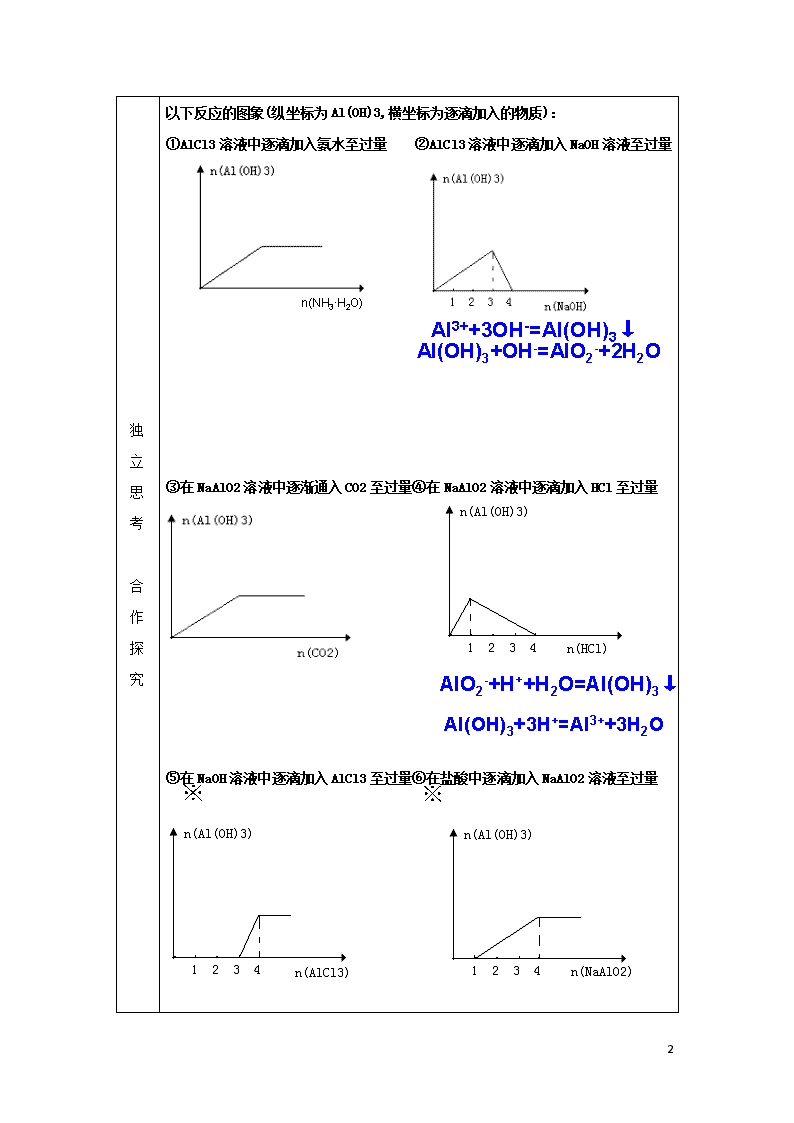
以下反应的图象(纵坐标为Al(OH)3,横坐标为逐滴加入的物质):
①AlCl3溶液中逐滴加入氨水至过量 ②AlCl3溶液中逐滴加入NaOH溶液至过量
③在NaAlO2溶液中逐渐通入CO2至过量④在NaAlO2溶液中逐滴加入HCl至过量
⑤在NaOH溶液中逐滴加入AlCl3至过量⑥在盐酸中逐滴加入NaAlO2溶液至过量
3
典型例题:
将某质量的镁铝合金溶解在500mL盐酸中,然后取出10mL溶液用1mol/LNaOH溶液滴定,产生沉淀质量与碱溶液的关系.求:
(1)合金中镁和铝的物质的量之比. 3:1
(2)盐酸的物质的量浓度(假设反应后溶液体积不变) 0.2mol/L
巩
固
练
习
1、在100mL1mol/LAlCl3溶液中,加入多少体积的0.5mol/LNaOH溶液可以得到6.24g沉淀? 480mL或640mL
2、现有镁铝混合粉末10.2g,将它溶解在500mL4mol/LHCl里,若要使沉淀质量达到最大值,则需要加入2mol/L的NaOH溶液的体积为多少?
3