- 145.50 KB
- 2021-05-13 发布
四川省广安市岳池县第一中学2019-2020学年高一6月月考(期中)试题
可能用到的原子量: H:1 C:12 O:16 Na:23 Al:27 Cl:35.5
第Ⅰ卷 选择题 (共50分)
一、选择题(每小题只有1个选项符合题意。本题包括25小题,每小题2分,共50分,)
1.下列元素中,不属于主族元素的是( )
A. 磷 B. 钙 C. 铁 D. 砹
2.下列物质的电子式书写正确的是( )
A. B. C. D.
3.科学家预测,月球的土壤中吸附着数百万吨3He,100吨3He核聚变释放的能量相当于目前人类一年消耗的能量。下列说法正确的是( )
A.3He的最外层电子数为2,具有较强的金属性 B.3He位于周期表第二周期第ⅡA族
C. 其原子核中质子数为2、中子数为1 D. 核聚变是化学反应
4. 元素的性质随着元素原子序数的递增而呈周期性变化的原因是( )
A.元素的金属性、非金属性呈周期性变化
B.元素的原子半径呈周期性变化
C.元素的化合价呈周期性变化
D.元素原子的核外电子排布呈周期性变化
5. 在元素周期表中金属与非金属的分界处,可以找到( )
A.合金材料 B.催化剂 C.农药 D.半导体材料
6.关于化学键的下列叙述中,正确的是( )
A. 离子化合物可能含共价键,共价化合物中一定不含离子键
B.共价化合物可能含离子键,离子化合物中只含离子键
C. 构成单质分子的微粒一定含有共价键
D. 在过氧化钠中,既存在离子键,又存在极性键
7. X和Y属短周期元素,X原子的最外层电子数是次外层电子数的一半,Y位于X的前一周期,且最外层只有一个电子,下列的说法正确的是:( )
A.X可能是第二周期非金属元素 B.X可能是第三周期金属元素
C.Y可能与X同主族 D.Y一定是金属元素
8.下列关于物质性质变化的比较,正确的是( )
A. 碱性强弱:KOH>NaOH>Mg(OH)2 B. 原子半径大小:Cl> Na>O
C. 稳定性:HI>HBr>HCl>HF D. 还原性强弱:Cl- > Br- > I-
9.下列说法正确的是( )
A. Li是最活泼金属,F是最活泼非金属 B. Mg(OH)2碱性比Ca(OH)2强
C. 元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16纵行
D. X2+的核外电子数目为18,则X在第四周期ⅡA族
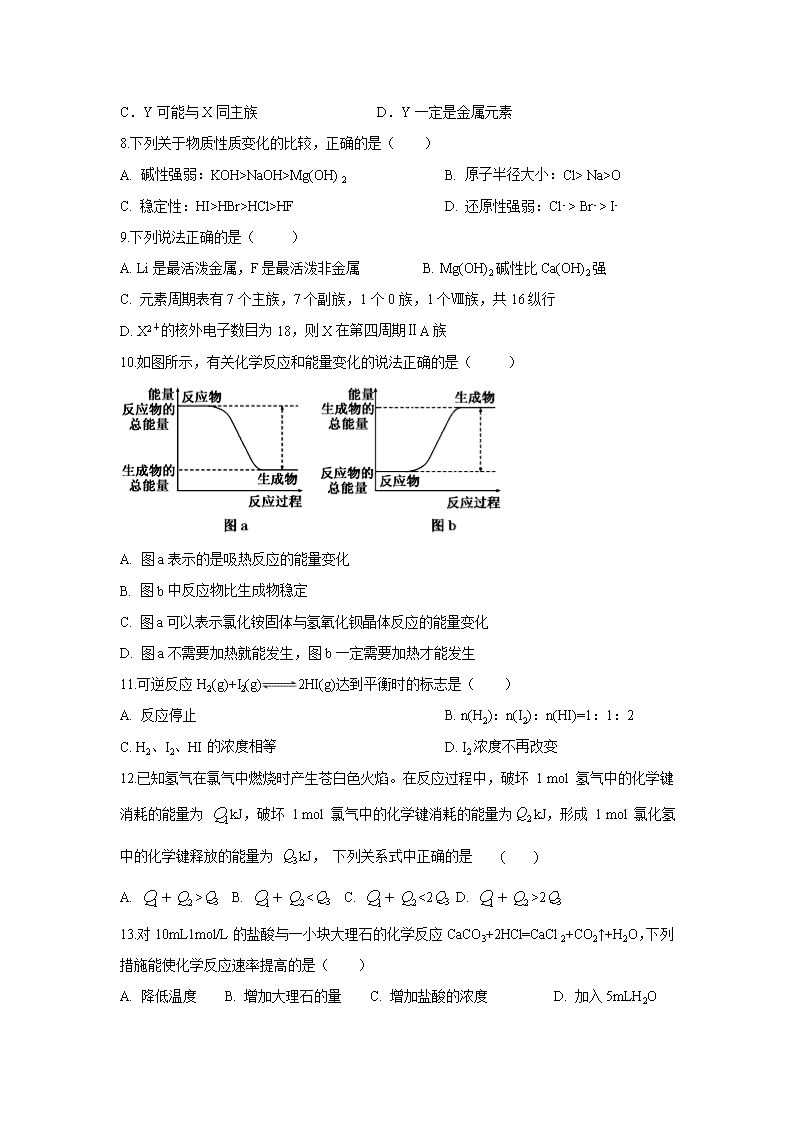
10.如图所示,有关化学反应和能量变化的说法正确的是( )
A. 图a表示的是吸热反应的能量变化
B. 图b中反应物比生成物稳定
C. 图a可以表示氯化铵固体与氢氧化钡晶体反应的能量变化
D. 图a不需要加热就能发生,图b一定需要加热才能发生
11.可逆反应H2(g)+I2(g)2HI(g)达到平衡时的标志是( )
A. 反应停止 B. n(H2):n(I2):n(HI)=1:1:2
C. H2、I2、HI的浓度相等 D. I2浓度不再改变
12.已知氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏 1 mol 氢气中的化学键消耗的能量为 kJ,破坏 1 mol 氯气中的化学键消耗的能量为kJ,形成 1 mol 氯化氢中的化学键释放的能量为 kJ, 下列关系式中正确的是 ( )
A. +> B. +< C. +<2 D. +>2
13.对10mL1mol/L的盐酸与一小块大理石的化学反应CaCO3+2HCl=CaCl2+CO2↑+H2O,下列措施能使化学反应速率提高的是( )
A. 降低温度 B. 增加大理石的量 C. 增加盐酸的浓度 D. 加入5mLH2O
14.反应A+3B═2C+2D在四种不同的情况下的反应速率如下,最快的是( )
A. v(A)=0.15mol/(L•min) B. v(B)=0.6mol/(L•min)
C. v(c)=0.4mol/(L•min) D. v(D)=0.45mol/(L•min)
15.在一密闭容器中进行反应:2SO2+O22SO3(g),已知反应过程中某一时刻SO2、O2和SO3浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1。当反应达到平衡时,可能存在的数据是( )
A. SO2为0.4 mol·L-1、O2为0.2 mol·L-1 B. SO2为0.3 mol·L-1
C. SO3为0.4 mol·L-1 D. SO2、SO3均为0.1 mol·L-1
16.下列物质中属于有机物的是( )
①酒精②食盐③石墨④甲烷⑤红糖⑥水⑦一氧化碳⑧石灰石⑨脂肪⑩纤维素
A. ①②④⑤⑨ B. ①④⑤⑨⑩
C. ①③④⑤⑦⑧⑨⑩ D. ①④⑤⑥⑩
17.下列分子式肯定属于烷烃的是( )
A.C8H16 B.C5H8 C.C7H16 D.C7Hl4
18.下列叙述错误的是( )
A. 通常情况下,甲烷跟强酸、强碱、强氧化剂不起反应
B. 甲烷是正四面体结构
C. 甲烷跟氯气反应无论生成CH3Cl、CH2Cl2、CHCl3,还是CCl4,都属于取代反应
D. 甲烷的四种取代物常温下均为液体
19.下列反应中,能够说明乙烯分子具有不饱和键的是( )
A. 燃烧反应 B. 取代反应 C. 加成反应 D. 化合反应
20.下列烷烃按沸点由高到低顺序排列正确的是( )
①正丁烷②异丁烷③正戊烷④异戊烷⑤新戊烷
A. ①②③④⑤ B. ⑤④③②①
C. ③①⑤④② D. ③④⑤①②
21.一定条件下能与苯发生化学反应的物质是( )
A. H2 B. 溴水
C. NaOH溶液 D. KMnO4酸性溶液
22. 山梨酸(CH3—CH=CH—CH=CH—COOH)是一种常用的食品防腐剂。下列关于山梨酸性质的叙述中,不正确的是( )。
A.可与钠反应 B.可与碳酸钠溶液反应
C.可与溴水溶液发生取代反应 D.分子中含有两种官能团
23.除去乙烷气体中的少量乙烯的最好方法是( )
A.在催化剂存在下与氢气反应 B.通过盛有溴水的洗气瓶
C.通过高锰酸钾酸性溶液 D.依次通过KMnO4(H+)、NaOH溶液
24.丁烷(C4H10)一氯代物C4H9Cl的同分异构体数目共有( )
A. 2种 B. 3种 C. 4种 D. 5种
25.一定量的甲烷燃烧产物为C0、C02和水蒸气,此混合气体重49.6g,当其缓慢通过无水CaCl2时,CaCl2增重25.2 g,则原混合气体中C0的质量为( )
A.11.2g B.13.2 g C.19.7 g D.24.4 g
第Ⅱ卷 非选择题 (共50分)
二、填空题(本题包括3小题,共50分)
26.(本题每空1分,共10分):
(1)酸性:H2SO4___HClO4;(用“>”、“<”、“=”填空)
(2)沸点:F2____Cl2,HF___HCl;(用“>”、“<”、“=”填空)
(3)热稳定性:CH4____NH3,HCl____HI。(用“>”、“<”、“=”填空)
(4)选择下列某种答案的序号, 填入下表的空格
①同位素 ②同素异形体 ③同分异构体 ④同系物 ⑤同种物质
物质
丁烷与
红磷
庚烷与
氯仿与
氕与
名称
2--甲基丙烷
与白磷
十六烷
三氯甲烷
氘、氚
相互
关系
27.(20分)Ⅰ.在800 ℃2 L密闭容器中,反应2NO+O22NO2,n(NO)随时间的变化如下表:
时间(s)
0
1
2
3
4
5
n(NO)/mol
0.020
0.010
0.008
0.007
0.007
0.007
(1)如图表示各物质浓度的变化曲线,
A点处,v(正)___________v(逆), A点正反应速率_________B点正反应速率。 (用“>”、“<”、“=”填空)
(2)图中表示O2变化的曲线是___________。用NO2表示从0~2 s内该反应的平均速率v=____________________________。
(3) 能使该反应的反应速率增大的是____________。
A.及时分离出NO2气体 B.升高温度
C.减小O2的浓度 D.选择高效的催化剂
(4) 能说明该反应已经达到平衡状态的是___________。
A.容器内压强保持不变 B.v(NO)=2v(O2)
C.容器内的密度保持不变 D.v逆(NO2)=2v正(O2)
Ⅱ.(1)相对分子质量为72的烷烃,此烷烃的分子式为________;
(2) 乙醇的官能团名称为________;
(3)苯与液溴取代反应的化学方程式_______________________________________;
(4)乙醇与乙酸酯化反应的化学方程式_______________________________________。
28.(20分)下表是元素周期表的一部分, 针对表中的①~⑨种元素,填写下列空白:
主族
周期
ⅠA
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
0族
2
①
②
③
3
④
⑤
⑥
⑦
⑧
4
⑨
(1) 在这些元素中,化学性质最不活泼的是: (填具体元素符号或化学式,下同)。
⑥元素的原子结构示意图是
(2) 在最高价氧化物的水化物中,酸性最强的化合物的分子式是____ ___,碱性最强的化合物的化学式是________ ____。
(3) 最高价氧化物是两性氧化物的元素是_____ ____;写出它最高价氧化物对应水化物与氢氧化钠反应的化学方程式_____ ___ __ _ 。
(4) 元素③与④形成淡黄色化合物的电子式: ,
该化合物属于 (填 “共价”或“离子”)化合物。
(5)用电子式表示③与①最高价态形成的化合物的形成过程 ,将标准状况下4.48L该化合物通入足量的③和④形成的淡黄色固体化合物中,充分反应后,固体的质量增加 g。
【参考答案】
第I卷(选择题,共50分)
题号
1
2
3
4
5
6
7
8
9
10
答案
C
D
C
D
D
A
C
A
D
B
题号
11
12
13
14
15
16
17
18
19
20
答案
D
C
C
D
B
B
C
D
C
D
题号
21
22
23
24
25
答案
A
C
B
C
A
第Ⅱ卷(非选择题,共50分)
26. (10分,每空1分)
(1)< (2)< > (3)< >
(4) ③②④⑤①
27. (20分,每空2分)
Ⅰ. (1)> > (2)d 0.003 mol·L-1·s-1 (3)BD (4) AD
Ⅱ.(1)C5H12
(2)羟基
(3)+Br2+HBr CH3COOH+CH3CH2OH C2H5OOCCH3+H2O
28.(20分,每空2分)
Ⅰ.(1)Ar
(2)HClO4 KOH
(3) Al NaOH+Al(OH)3===NaAlO2+H2O
(4) 离子
(5) 5.6