- 982.50 KB
- 2021-04-17 发布
第2课时 乙 酸
一、乙酸的组成、结构、物理性质与酸性
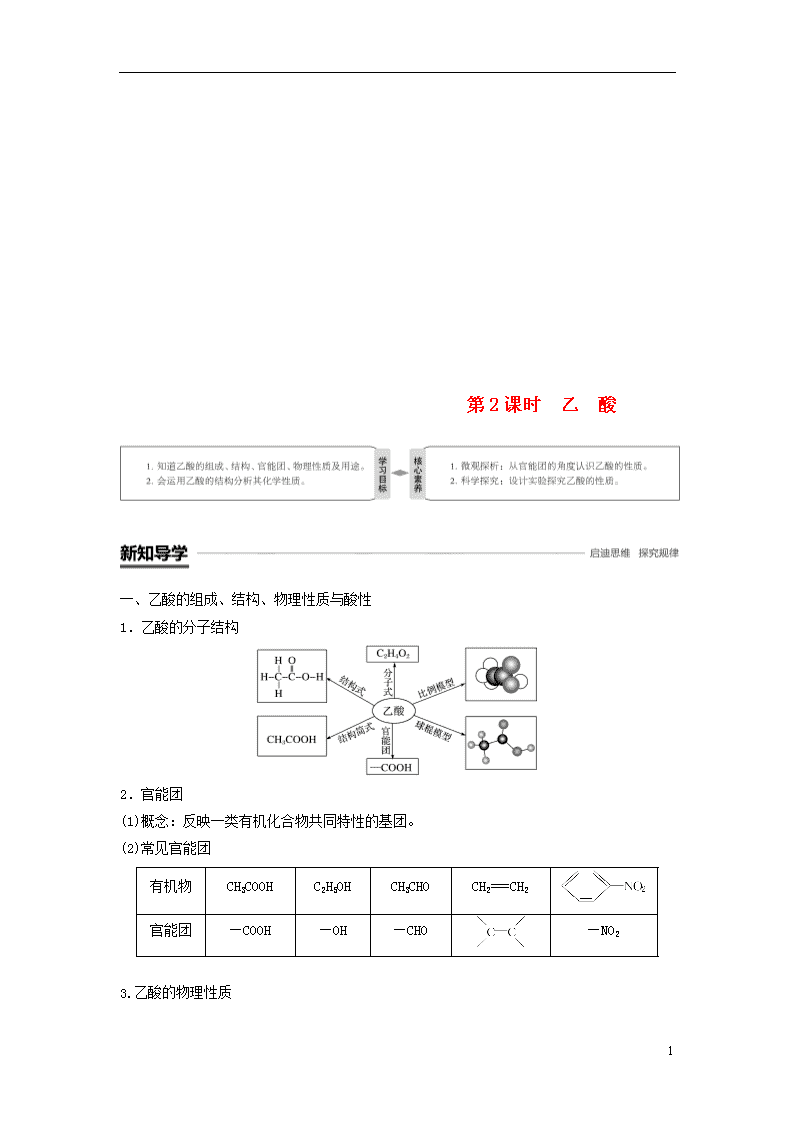
1.乙酸的分子结构
2.官能团
(1)概念:反映一类有机化合物共同特性的基团。
(2)常见官能团
有机物
CH3COOH
C2H5OH
CH3CHO
CH2===CH2
官能团
—COOH
—OH
—CHO
—NO2
3.乙酸的物理性质
16
(1)乙酸俗称醋酸,是一种有强烈刺激性气味的无色液体,易溶于水和乙醇。
(2)熔点:16.6 ℃,温度低于熔点时,乙酸凝结成晶体,所以纯净的乙酸又称冰醋酸。
4.乙酸的酸性
(1)乙酸是一元弱酸,具有酸的通性,写出乙酸与下列物质反应的离子方程式:
①Na:2Na+2CH3COOH===2CH3COO-+2Na++H2↑。
②NaOH:CH3COOH+OH-===CH3COO-+H2O。
③Na2O:2CH3COOH+Na2O===2CH3COO-+2Na++H2O。
④Na2CO3:2CH3COOH+CO===2CH3COO-+H2O+CO2↑。
(2)证明乙酸的酸性比碳酸强的方法
乙酸与碳酸、水和乙醇中羟基氢的活泼性比较
乙醇
水
碳酸
乙酸
羟基氢的活泼性
酸碱性
中性
中性
弱酸性
弱酸性
与Na
反应
反应
反应
反应
与NaOH
不反应
不反应
反应
反应
与NaHCO3
不反应
不反应
不反应
反应
例1 下列物质中不能用来区分乙酸、乙醇、苯的是( )
A.金属钠 B.溴水
C.碳酸钠溶液 D.紫色石蕊溶液
答案 B
解析 A项,钠与乙酸反应快于钠与乙醇的反应,苯不与Na反应,能区别;B项,溴水与乙醇、乙酸互溶,与苯萃取而使溴水层颜色变浅,不能区别;C项,Na2CO3溶液与乙酸放出CO2气体,与乙醇混溶,与苯分层,能区分;D项,紫色石蕊溶液与乙酸混合变红色,与乙醇混溶,与苯分层,能区分。
规律总结
鉴别乙醇和乙酸一般选用紫色石蕊溶液、NaHCO3溶液、Na2CO3溶液、氢氧化铜悬浊液,氧化铜粉末也能区别乙醇和乙酸。乙酸能与氢氧化铜和氧化铜反应,而乙醇不能。
16
例2 苹果酸的结构简式为。下列说法正确的是( )
A.苹果酸中能发生酯化反应的官能团有2种
B.1 mol苹果酸可与3 mol NaOH发生中和反应
C.1 mol苹果酸与足量金属Na反应生成1 mol H2
D.HOOC—CH2—CH(OH)—COOH与苹果酸互为同分异构体
答案 A
解析 苹果酸分子中含有羟基和羧基两种官能团,都能发生酯化反应,A项正确;羟基不能与NaOH发生中和反应,故1 mol苹果酸可与2 mol NaOH发生中和反应,B项错误;羟基和羧基均能与金属Na反应,故1 mol苹果酸与足量金属钠反应生成1.5 mol H2,C项错误;苹果酸的结构简式可写为或,即二者为同一物质,D项错误。
规律总结——羟基、羧基个数与生成气体的定量关系
(1)Na可以和所有的羟基反应,且物质的量的关系为2Na~2—OH~H2。
(2)Na2CO3、NaHCO3和—COOH反应产生CO2,物质的量的关系为Na2CO3~2—COOH~CO2,NaHCO3~—COOH~CO2。
二、乙酸的酯化反应
1.实验探究
(1)实验现象:饱和碳酸钠溶液的液面上有透明的不溶于水的油状液体产生,且能闻到香味。
(2)化学方程式:
。
2.酯化反应
(1)概念:酸与醇作用生成酯和水的反应。
(2)反应机理:酸脱羟基醇脱氢。
16
例3 将1 mol乙醇(其中的羟基氧用18O标记)在浓硫酸存在并加热下与足量乙酸充分反应。下列叙述不正确的是( )
A.生成的水分子中一定含有18O
B.生成的乙酸乙酯中含有18O
C.可能生成45 g乙酸乙酯
D.不可能生成相对分子质量为88的乙酸乙酯
答案 A
解析 CH3CH218OH与CH3COOH发生酯化反应的原理为CH3CH218OH+CH3COOH+H2O,因此生成的水中不含18O原子,乙酸乙酯中含有18O原子,生成乙酸乙酯的相对分子质量为90。该反应为可逆反应,1 mol CH3CH218OH参加反应,生成酯的物质的量为0
相关文档
- 2018秋高中语文第二单元第5课《张2021-04-17 16:57:046页
- 高中生物二轮必修模块典题精练722021-04-17 16:56:509页
- 2019-2020高中化学(人教版 选修4)练2021-04-17 16:56:3511页
- 湖北省宜昌市部分示范高中教学协作2021-04-17 16:54:529页
- 高中化学鲁科版选修3课后练习:1-1-22021-04-17 16:54:183页
- 2019-2020学年高中物理第六章传感2021-04-17 16:53:1310页
- 高中生物综合检测卷(必修1)2021-04-17 16:52:258页
- 精编20XX高中新生军训后的心得体会2021-04-17 16:52:008页
- 高中毕业生档案自我鉴定4篇2021-04-17 16:49:513页
- 2020版高中语文 专题2 获得教养的2021-04-17 16:49:466页