- 182.15 KB
- 2021-04-13 发布
初中化学·人教版·九年级下册——第十单元 酸和碱
课题 2 酸和碱的中和反应
第 1 课时 中和反应
测试时间:20 分钟
一、选择题
1.下列反应中属于中和反应的是( )
A.Fe+2HCl FeCl2+H2↑
B.BaCO3+2HCl BaCl2+H2O+CO2↑
C.2KOH+H2SO4 K2SO4+2H2O
D.2NaOH+CuCl2 Cu(OH)2↓+2NaCl
2.(2019 江苏常州模拟)下列处理废水的方法利用了中和反应原理的是( )
A.用石灰水处理尾气中的 SO2
B.用臭氧处理废水中的氧化物
C.用铁粉处理酸性废水
D.用熟石灰处理废水中的酸
3.(2019 上海浦东新区二模)关于中和反应的说法错误的是( )
A.一定放热 B.反应物一定是酸和碱
C.一定有水生成 D.生成的盐一定可溶
4.小烧杯中盛有含石蕊的稀盐酸。逐滴加入氢氧化钠溶液至过量,烧杯中溶液颜色变化的顺序是
( )
A.紫色→红色→蓝色 B.红色→紫色→蓝色
C.蓝色→红色→紫色 D.紫色→蓝色→红色
5.(2019 广西梧州二模)在滴有酚酞的氢氧化钠溶液中,逐滴滴加稀盐酸至过量,下列说法错误的是
( )
A.溶液 pH 逐渐变小
B.最后得到的溶液中只含有一种溶质
C.溶液颜色由红色逐渐变浅,最后变无色
D.生成的氯化钠质量逐渐增多,最后保持不变
6.(2019 云南红河一模)某同学用盐酸与氢氧化钠按照如图所示的方式进行中和反应实验。溶液由红
色变为无色。以下证明盐酸过量的操作及实验现象的叙述正确的是( )
A.滴加石蕊溶液,搅拌,溶液变蓝
B.滴加少量氢氧化钠溶液,搅拌,溶液变红色
C.加入蒸馏水,搅拌,溶液颜色不变
D.加入 Zn 片,产生气泡
7.(2019 湖北武汉模拟)化学兴趣小组的同学进行中和反应的实验,向一定量氢氧化钠溶液中滴加酚酞
溶液,溶液变红,再加入一定量稀盐酸,溶液由红色变为无色。下列说法不正确的是( )
A.溶液由红色变为无色,说明氢氧化钠和盐酸发生了化学反应
B.加入一定量稀盐酸后,所得溶液一定呈中性
C.滴加酚酞溶液后溶液变红,说明氢氧化钠溶液呈碱性
D.将稀盐酸换为稀硫酸,也能达到实验目的
二、填空题
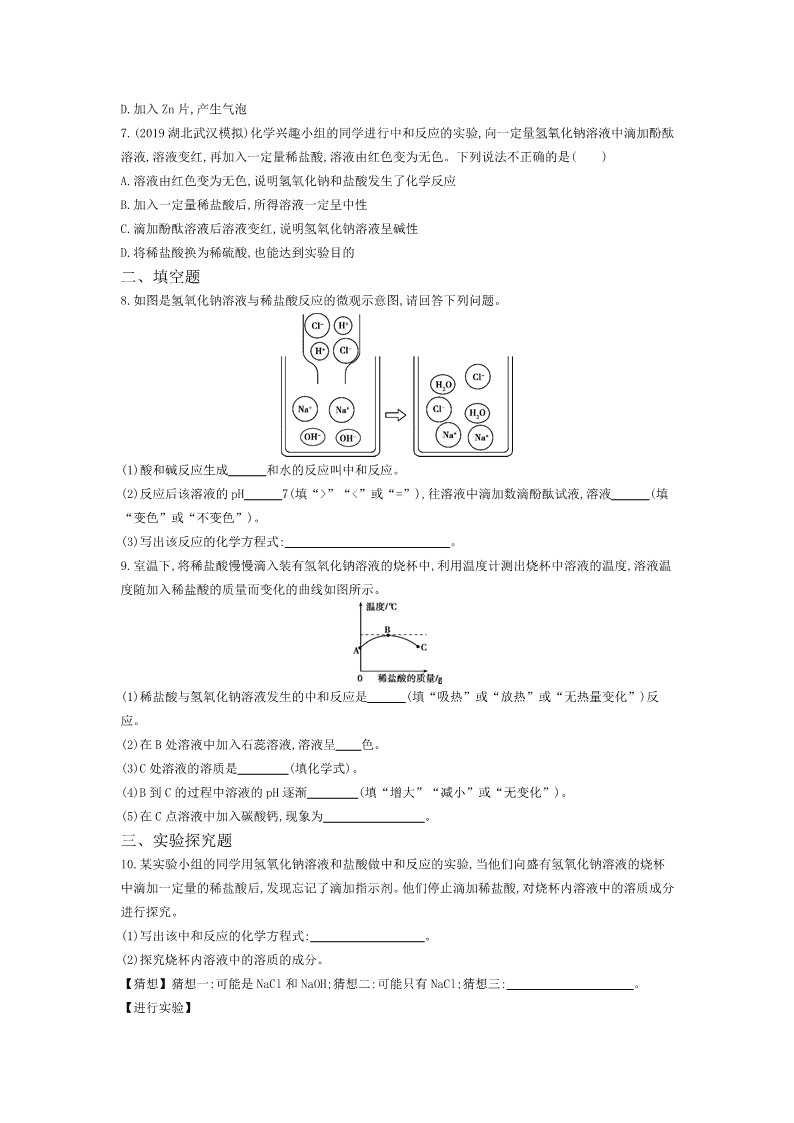
8.如图是氢氧化钠溶液与稀盐酸反应的微观示意图,请回答下列问题。
(1)酸和碱反应生成 和水的反应叫中和反应。
(2)反应后该溶液的 pH 7(填“>”“<”或“=”),往溶液中滴加数滴酚酞试液,溶液 (填
“变色”或“不变色”)。
(3)写出该反应的化学方程式: 。
9.室温下,将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,利用温度计测出烧杯中溶液的温度,溶液温
度随加入稀盐酸的质量而变化的曲线如图所示。
(1)稀盐酸与氢氧化钠溶液发生的中和反应是 (填“吸热”或“放热”或“无热量变化”)反
应。
(2)在 B 处溶液中加入石蕊溶液,溶液呈 色。
(3)C 处溶液的溶质是 (填化学式)。
(4)B 到 C 的过程中溶液的 pH 逐渐 (填“增大”“减小”或“无变化”)。
(5)在 C 点溶液中加入碳酸钙,现象为 。
三、实验探究题
10.某实验小组的同学用氢氧化钠溶液和盐酸做中和反应的实验,当他们向盛有氢氧化钠溶液的烧杯
中滴加一定量的稀盐酸后,发现忘记了滴加指示剂。他们停止滴加稀盐酸,对烧杯内溶液中的溶质成分
进行探究。
(1)写出该中和反应的化学方程式: 。
(2)探究烧杯内溶液中的溶质的成分。
【猜想】猜想一:可能是 NaCl 和 NaOH;猜想二:可能只有 NaCl;猜想三: 。
【进行实验】
实验步骤 实验操作 实验现象 结论
① 取少量烧杯内的溶液于试管中,滴入几滴酚酞试液,振荡 猜想一不成立
② 取少量烧杯内的溶液于另一支试管中,滴加碳酸钠溶液 猜想三成立
答案
一、选择题
1.答案 C 酸与碱发生反应生成盐与水的反应属于中和反应,四个选项中只有 C 属于中和反应。
2.答案 D 用熟石灰处理废水中的酸,是酸与碱之间生成盐和水的反应,利用了中和反应的原理。
3.答案 D 中和反应属于放热反应,一定放热;中和反应是酸与碱作用生成盐和水的反应,反应物是
酸和碱;中和反应是酸与碱作用生成盐和水的反应,一定有水生成;生成的盐不一定是可溶的,如硫酸
与氢氧化钡溶液反应生成硫酸钡白色沉淀。
4.答案 B 紫色石蕊溶液遇酸性溶液变红,遇碱性溶液变蓝,故含石蕊的稀盐酸显红色;氢氧化钠溶
液显碱性,逐滴加入氢氧化钠溶液,至恰好完全反应时,溶液显中性,颜色变为紫色;继续滴加氢氧化钠
溶液,溶液显碱性,颜色变为蓝色。
5.答案 B 随着氢氧化钠不断加入,溶液碱性减弱,pH 逐渐变小;最后得到的溶液中溶质是氯化钠和
氯化氢;溶液颜色由红色逐渐变浅,最后变无色;随着反应的进行,生成的氯化钠质量逐渐增大,完全反
应后氯化钠质量不再变化。
6.答案 D A 项,滴加石蕊溶液,搅拌,溶液变蓝,说明溶液显碱性,氢氧化钠有剩余;B 项,若溶液显中
性,滴加少量氢氧化钠溶液,搅拌,溶液也会变红色;C 项,加入蒸馏水,搅拌,溶液颜色不变,溶液可能显
酸性或中性;D 项,加入 Zn 片,产生气泡,是因为锌与稀盐酸反应生成氯化锌溶液和氢气,可证明盐酸过
量。
7.答案 B 溶液由红色变为无色,说明氢氧化钠和盐酸发生了化学反应;加入一定量稀盐酸后,所得
溶液不一定呈中性,也可能呈酸性;滴加酚酞溶液后溶液变红,说明氢氧化钠溶液呈碱性;将稀盐酸换
为稀硫酸,也能达到实验目的。
二、填空题
8.答案 (1)盐 (2)= 不变色 (3)NaOH+HCl NaCl+H2O
解析 (1)中和反应是酸与碱作用生成盐和水的反应。(2)由反应的微观示意图可知,反应后的溶液中
含有钠离子、氯离子和水分子,显中性,该溶液的 pH=7;往溶液中滴加数滴酚酞试液,溶液不变色。(3)
稀盐酸与氢氧化钠反应生成氯化钠和水。
9.答案 (1)放热 (2)紫 (3)NaCl 和 HCl (4)减小 (5)固体溶解,且产生气泡
解析 (1)由图像可以看出,随着稀盐酸的加入,温度在逐渐升高,说明稀盐酸与氢氧化钠溶液发生的
反应是放热反应。(2)B 点的温度最高,说明氢氧化钠与稀盐酸此时恰好完全中和,溶液显中性,滴加石
蕊溶液显示紫色。(3)B 点的温度最高,说明氢氧化钠与稀盐酸此时恰好完全中和,此时溶液中的溶质
是氯化钠,B 到 C 的过程中持续滴加稀盐酸,则酸过量。(4)B 到 C 的过程中,反应结束后继续滴加稀盐
酸,溶液由中性转化为酸性。(5)C 点的溶液显酸性,加入碳酸钙后,其中的碳酸钙与稀盐酸反应生成氯
化钙、水和二氧化碳,固体逐渐消失,并产生气泡。
三、实验探究题
11.答案 (1)NaOH+HCl NaCl+H2O (2)【猜想】可能是 NaCl 和 HCl 【进行实验】①溶液不变色
②产生气泡
解析 (1)氢氧化钠和稀盐酸反应生成氯化钠和水,该中和反应的化学方程式为 NaOH+HCl
NaCl+H2O。(2)【猜想】如果氢氧化钠过量,则溶质是氯化钠和氢氧化钠,如果稀盐酸和氢氧化钠恰好
完全反应,则溶质是氯化钠,如果稀盐酸过量,则溶质是氯化钠和氯化氢。【进行实验】①取少量烧杯
内的溶液于试管中,滴入几滴酚酞试液,振荡,溶液不变色,说明溶液中不含有氢氧化钠,猜想一不成
立;②取少量烧杯内的溶液于另一支试管中,滴加碳酸钠溶液,产生气泡,说明溶液中含有稀盐酸,猜想
三成立。
相关文档
- 新人教版初中化学课后达标训练10-22021-04-13 21:02:2211页
- 2019九年级化学全册 第二单元 常见2021-04-13 19:24:059页
- 酸和碱的反应 教案2021-04-12 22:00:103页
- 北京专版2020中考化学复习方案主题2021-04-12 16:23:1812页
- 人教版九年级化学第10单元 酸和碱2021-04-12 16:21:25109页
- 人教版化学九下《常见的酸和碱(三)》2021-04-12 15:02:562页
- 人教版化学九年级下册第10单元常见2021-04-12 12:26:194页
- 常见的酸和碱学案2021-02-27 08:55:094页
- 2019届中考化学复习 第十讲 酸和碱2021-02-26 22:34:506页
- 九年级化学下册第十单元酸和碱课题2021-02-26 22:32:184页