- 590.00 KB
- 2021-05-20 发布
- 1、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 2、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报QQ:3215808601
金属的腐蚀与防护
(40分钟 70分)
一、选择题(本题包括9小题,每小题6分,共54分)
1.家用炒菜锅用水清洗放置后,出现红棕色的锈斑。在此变化过程中不发生的化学反应是 ( )
A.4Fe(OH)2+2H2O+O24Fe(OH)3
B.2Fe+2H2O+O22Fe(OH)2
C.2H2O+O2+4e-4OH-
D.Fe-3e-Fe3+
【解析】选D。家用炒菜锅中Fe、C构成原电池的两极。用水清洗放置后,出现红棕色的锈斑是因为在潮湿的环境中铁发生电化学腐蚀。负极:Fe-2e-Fe2+,正极:2H2O+O2+4e-4OH-,总反应:2Fe+2H2O+O22Fe(OH)2,生成的Fe(OH)2不稳定又被空气中的氧气氧化为红褐色的Fe(OH)3,反应化学方程式为4Fe(OH)2+O2+2H2O4Fe(OH)3,Fe(OH)3能分解生成铁锈。A、B、C正确。
2.(2020·襄阳高二检测)下列有关金属腐蚀的说法中正确的是 ( )
A.金属腐蚀指不纯金属与接触到的电解质溶液进行化学反应而损耗的过程
B.电化学腐蚀指在外加电流的作用下不纯金属发生化学反应而损耗的过程
C.钢铁腐蚀最普遍的是吸氧腐蚀,负极吸收氧气,产物最终转化为铁锈
D.金属的电化学腐蚀和化学腐蚀本质相同,但电化学腐蚀伴有电流产生
【解析】选D。金属腐蚀的本质,主要是金属原子失电子被氧化,腐蚀的内因是金属的化学性质比较活泼,外因是金属与空气、水或其他腐蚀性的物质接触,腐蚀主要包括化学腐蚀和电化学腐蚀,所以A错误;电化学腐蚀指不纯金属与电解质溶液接触时发生原电池反应而损耗的过程,不需要外加电流,所以B错误;钢铁腐蚀最普遍的是吸氧腐蚀,正极吸收氧气,所以C错误。
3.(2020·西城区高二检测)我国某大城市今年夏季多次降下酸雨。据环保部门测定,该城市整个夏季酸雨的pH平均值为3.2。在这种环境中的铁制品极易被腐蚀。对此条件下铁的腐蚀的叙述不正确的是 ( )
- 10 -
A.此腐蚀过程有化学腐蚀也有电化学腐蚀
B.发生电化学腐蚀时,正极反应式为2H2O+O2+4e-4OH-
C.在电化学腐蚀过程中有氢气产生
D.发生电化学腐蚀时,负极反应式为Fe-2e-Fe2+
【解析】选B。在铁制品的腐蚀中,金属铁可以和溶液中的氢离子直接发生化学腐蚀,铁制品中含有铁和碳,再加之电解质环境,具备了原电池的构成条件,也会发生电化学腐蚀,故A正确;发生电化学腐蚀时,碳作正极,溶液中的氢离子得电子生成氢气,正极反应式为2H++2e-H2↑,故B错误,C正确;发生电化学腐蚀时,铁作负极,电极反应式为Fe-2e-Fe2+,故D正确。
4.(2020·合肥高二检测)下列说法中,不正确的是 ( )
A
B
C
D
钢铁表面水膜的酸性很弱或呈中性,发生吸氧腐蚀
钢铁表面水膜的酸性较强,发生析氢腐蚀
将锌板换成铜板对钢闸门保护效果更好
钢闸门作为阴极而受到保护
【解析】选C。钢铁是铁碳合金,当表面水膜为弱酸性或中性溶液时,易发生吸氧腐蚀,故A正确;钢铁是铁碳合金,当表面水膜为酸性较强时,易发生析氢腐蚀,故B正确;Zn-Fe原电池,Fe为正极,可减缓腐蚀,如果换成Fe-Cu原电池,Fe为负极,可加快钢闸门的腐蚀,故C错误;通过连接外接电源的负极保护钢闸门不受腐蚀,这是阴极电保护法,故D正确。
【补偿训练】
(2020·平顶山高二检测)下列金属防腐的措施中,使用阴极电保护法的是( )
A.水中的钢闸门连接电源的负极
B.金属护栏表面涂漆
C.汽车底盘喷涂高分子膜
D.地下钢管连接镁块
【解析】选A。水中的钢闸门连接电源的负极,钢闸门为阴极,从而得以保护,A项正确;金属护栏表面涂漆的原理是隔绝金属护栏与空气接触,从而减缓金属护栏的腐蚀,B项错误;汽车底盘喷涂高分子膜的原理也是隔绝与空气的接触,C项错误;地下钢管连接镁块,形成了原电池,属于牺牲阳极保护法,D项错误。
- 10 -
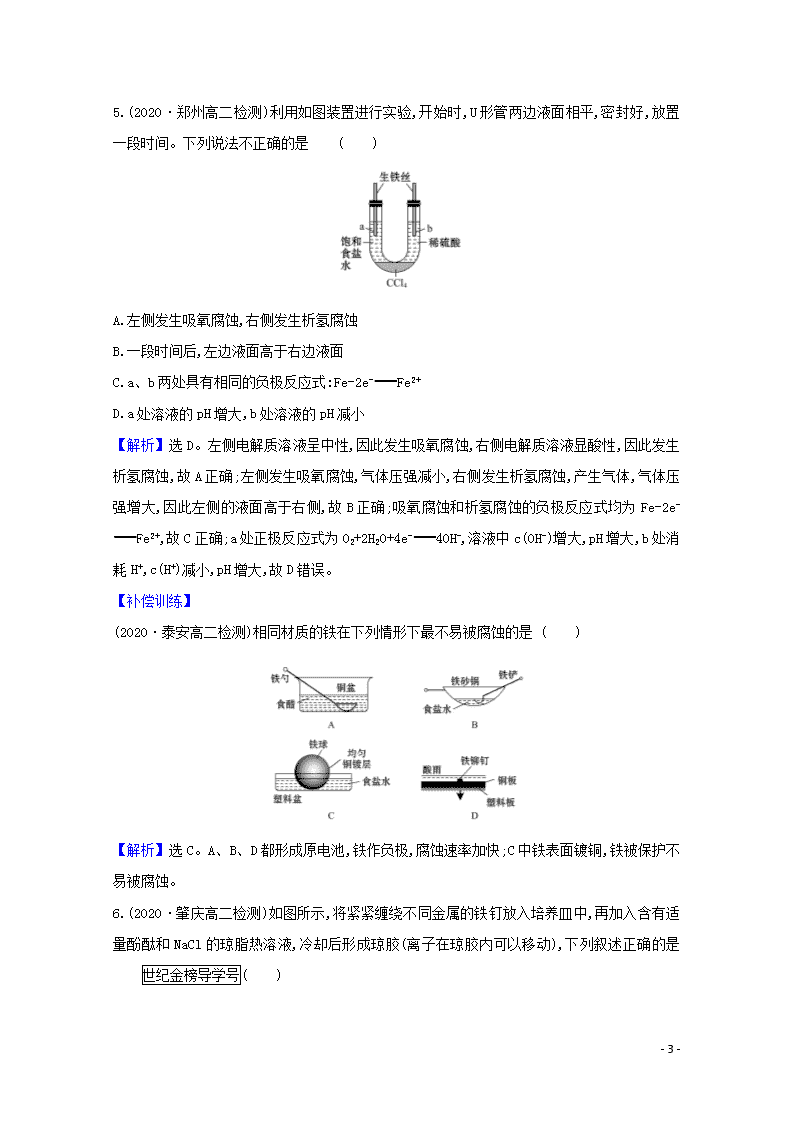
5.(2020·郑州高二检测)利用如图装置进行实验,开始时,U形管两边液面相平,密封好,放置一段时间。下列说法不正确的是 ( )
A.左侧发生吸氧腐蚀,右侧发生析氢腐蚀
B.一段时间后,左边液面高于右边液面
C.a、b两处具有相同的负极反应式:Fe-2e-Fe2+
D.a处溶液的pH增大,b处溶液的pH减小
【解析】选D。左侧电解质溶液呈中性,因此发生吸氧腐蚀,右侧电解质溶液显酸性,因此发生析氢腐蚀,故A正确;左侧发生吸氧腐蚀,气体压强减小,右侧发生析氢腐蚀,产生气体,气体压强增大,因此左侧的液面高于右侧,故B正确;吸氧腐蚀和析氢腐蚀的负极反应式均为Fe-2e-Fe2+,故C正确;a处正极反应式为O2+2H2O+4e-4OH-,溶液中c(OH-)增大,pH增大,b处消耗H+,c(H+)减小,pH增大,故D错误。
【补偿训练】
(2020·泰安高二检测)相同材质的铁在下列情形下最不易被腐蚀的是 ( )
【解析】选C。A、B、D都形成原电池,铁作负极,腐蚀速率加快;C中铁表面镀铜,铁被保护不易被腐蚀。
6.(2020·肇庆高二检测)如图所示,将紧紧缠绕不同金属的铁钉放入培养皿中,再加入含有适量酚酞和NaCl的琼脂热溶液,冷却后形成琼胶(离子在琼胶内可以移动),下列叙述正确的是 世纪金榜导学号( )
- 10 -
A.a中铁钉附近呈现红色
B.b中铁钉上发生还原反应
C.a中铜丝上发生氧化反应
D.b中铝条附近有气泡产生
【解析】选B。a、b均构成原电池,a中Fe为负极,铜丝为正极,发生O2+2H2O+4e-4OH-,故a中铜丝处变红,b中Al为负极,Fe为正极,附近有OH-生成,故B项正确。
7.(2020·绍兴高二检测)将一根较纯铁棒垂直没入水中,由于深水处溶氧量较少,一段时间后发现AB段产生较多铁锈,BC段腐蚀严重,下列关于此现象的说法错误的是 ( )
A.铁棒AB段发生的反应为O2+2H2O+4e-4OH-
B.腐蚀过程中在铁棒上会产生微电流,且方向是从AB段到BC段
C.向水中加入一定量硫酸钾固体后,对铁棒的生锈速率几乎无影响
D.产生这种现象的本质是铁棒所处的化学环境不同
【解析】选C。铁在水中发生吸氧腐蚀,BC段作原电池负极,AB段作原电池正极,正极发生反应O2+2H2O+4e-4OH-,故A项正确;腐蚀过程中电子从BC段流向AB段,电流方向为从AB段到BC段,故B项正确;向水中加入一定量的硫酸钾固体后,离子浓度增大,铁棒的生锈速率增大,故C项错误;此原电池的构成是由于铁棒所处的化学环境不同,故D项正确。
【补偿训练】
(2020·长沙高二检测)铜板上的铁铆钉处的吸氧腐蚀原理如图所示,下列有关说法不正确的是 ( )
A.正极的电极反应为2H++2e-H2↑
- 10 -
B.此过程中还涉及的反应:4Fe(OH)2+2H2O+O24Fe(OH)3
C.此过程中铜并不被腐蚀
D.此过程中电子从Fe流向Cu
【解析】选A。吸氧腐蚀的电极反应:负极:2Fe-4e-2Fe2+,正极:O2+2H2O+4e-
4OH-,溶液中发生反应:Fe2++2OH-Fe(OH)2↓,Fe(OH)2继续被氧化:4Fe(OH)2+
2H2O+O24Fe(OH)3,Fe(OH)3脱去一部分水形成铁锈。
8.糕点包装中常用的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是 ( )
A.脱氧过程是吸热反应,可降低温度,延长糕点保质期
B.脱氧过程中铁作原电池正极,电极反应:Fe-3e-Fe3+
C.脱氧过程中碳作原电池负极,电极反应:2H2O+O2+4e-4OH-
D.含有1.12 g铁粉的脱氧剂,理论上最多能吸收氧气336 mL(标准状况)
【解析】选D。钢铁腐蚀中铁作负极,碳作正极,B、C错误;n(Fe)=0.02 mol,负极电极反应式:2Fe-4e-2Fe2+,生成的Fe2+与正极生成的OH-结合生成Fe(OH)2,Fe(OH)2被空气中的氧气氧化生成Fe(OH)3,所以0.02 mol Fe最终失去0.06 mol电子,消耗n(O2)==0.015 mol,标准状况下为336 mL,D正确。
9.(2020·成都高二检测)利用如图装置探究铁在海水中的电化学腐蚀与防护。下列说法不正确的是 ( )
世纪金榜导学号
A.若X为锌棒,开关K置于M处,可减缓铁的腐蚀,采用了牺牲阳极保护法
B.若X为锌棒,开关K置于N处,X极的反应:4OH--4e-O2↑+2H2O
C.若X为碳棒,开关K置于N处,可减缓铁的腐蚀,采用了阴极电保护法
- 10 -
D.若X为碳棒,开关K置于M处,X极的反应:O2+4e-+2H2O4OH-
【解析】选B。X为锌棒,K位于M时,为原电池,锌为负极,被腐蚀,保护了铁,A对;X为锌棒,开关K置于N处,为电解池,锌棒为阳极:Zn-2e-Zn2+,B错;若X为碳棒,开关K置于N处,为电解池,铁棒作阴极,被保护,C对;若X为碳棒,开关K置于M处,为原电池,发生吸氧腐蚀,X极:O2+4e-+2H2O4OH-,D对。
二、非选择题(本题包括1小题,共16分)
10.(2020·石家庄高二检测)根据如图装置,回答下列问题。
(1)C中Fe极的电极反应式为 _________________________________。
(2)B中Fe极的电极反应式为 _________________________________,
Cu极附近溶液的pH____________(填“增大”“减小”或“不变”)。
比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是_____________________。
【解析】(1)装置C中Zn-Fe-稀硫酸构成原电池,其中Zn作负极,电极反应式为Zn-2e-Zn2+,Fe作正极,电极反应式为2H++2e-H2↑。
(2)装置B中,Cu-Fe-海水构成原电池,其中负极(Fe):2Fe-4e-2Fe2+,正极(Cu):2H2O+O2+4e-4OH-。该装置本质上是发生的吸氧腐蚀,故Cu极附近c(OH-)增大,pH增大。铁被腐蚀的快慢顺序为B>A>C。
答案:(1)2H++2e-H2↑ (2)2Fe-4e-2Fe2+ 增大 B>A>C
【补偿训练】
(2020·青岛高二检测)如何防止铁的锈蚀是工业上研究的重点内容。为研究铁锈蚀的影响因素,某同学做了如下探究实验:
序号
内容
实验现象
1
常温下将铁丝放在干燥的空气中一个月
干燥的铁丝表面依然光亮
2
常温下将铁丝放在潮湿的空气中一小时
铁丝表面依然光亮
3
常温下将铁丝放在潮湿的空气中一个月
铁丝表面已变得灰暗
4
将潮湿的铁丝放在常温下的氧气流中一小时
铁丝表面略显灰暗
- 10 -
5
将潮湿的铁丝放在高于常温的氧气流中一小时
铁丝表面已变得灰暗
6
将浸过氯化钠溶液的铁丝放在高于常温的氧气流中一小时
铁丝表面灰暗程度比实验5严重
请回答以下问题:
(1)上述实验中发生了电化学腐蚀的是____________(填序号);在电化学腐蚀中,负极反应是_____________________________________________,
正极反应是 _____________________________________________。
(2)由该实验可知,影响铁锈蚀速率的因素是 ___。
(3)为防止铁的锈蚀,工业上普遍采用的方法是________________________(答两种方法)。
【解析】(1)只要铁丝表面变暗则发生了腐蚀,由实验现象(铁丝表面变灰暗)得出发生了电化学腐蚀的实验为3、4、5、6。
(2)实验内容中进行对比的湿度、温度、O2的浓度(氧气流与空气)、电解质溶液(NaCl溶液)等条件就是影响铁锈蚀速率的因素。
(3)从改变物质的内部结构方面及覆盖保护层、原电池原理等方面进行思考。
答案:(1)3、4、5、6 Fe-2e-Fe2+(或2Fe-4e-2Fe2+) 2H2O+O2+4e-4OH-
(2)湿度、温度、O2的浓度、电解质的存在
(3)电镀、喷油漆、喷镀等表面覆盖保护层,牺牲阳极保护法等(其他答案合理即可)
(20分钟 30分)
一、选择题(本题包括2小题,每小题6分,共12分)
11.(2018·北京高考)验证牺牲阳极保护法,实验如下(烧杯内均为经过酸化的 3% NaCl 溶液)。
①
②
③
在Fe表面生
成蓝色沉淀
试管内无
明显变化
试管内生成
蓝色沉淀
下列说法不正确的是 ( )
A.对比②③,可以判定Zn保护了Fe
B.对比①②,K3[Fe(CN)6]可能将Fe氧化
C.验证Zn保护Fe时不能用①的方法
- 10 -
D.将Zn换成Cu,用①的方法可判断Fe比Cu活泼
【解析】选D。根据实验②的现象可知,在酸化的3%NaCl溶液中Fe电极未溶解,根据实验③的现象可知,Fe在酸化的3%NaCl溶液生成了Fe2+,两者对照,可以判定Zn保护了Fe,A正确;根据实验②取出Fe附近的溶液,滴加K3[Fe(CN)6]溶液,无明显变化,可知Fe电极附近未生成Fe2+,而实验①中Fe表面变蓝,说明K3[Fe(CN)6]可能将Fe氧化,B、C正确;将Zn换成Cu,用①的方法K3[Fe(CN)6]可将Fe氧化,Fe表面也会生成蓝色沉淀,不能根据电化学原理判断Fe比Cu活泼。
【延伸探究】
实验③中金属铁发生的腐蚀是吸氧腐蚀还是析氢腐蚀?写出相关的电极反应式。
提示:析氢腐蚀。由于电解质溶液是酸化的 3% NaCl溶液,因此发生析氢腐蚀,电极反应式为Fe-2e-Fe2+(负极),2H++2e-H2↑(正极)。
12.(2020·牡丹江高二检测)用压强传感器探究生铁在pH=2和pH=4的醋酸溶液中发生腐蚀的装置及得到的图象如下。分析图象,以下结论错误的是 ( )
世纪金榜导学号
A.溶液pH≤2时,生铁发生析氢腐蚀
B.在酸性溶液中生铁可能发生吸氧腐蚀
C.析氢腐蚀和吸氧腐蚀的速率一样快
D.两溶液中负极反应均为Fe-2e-Fe2+
【解析】选C。根据pH=2时锥形瓶中气体压强与时间的关系知,压强随着反应的进行而逐渐增大,说明该装置中发生了析氢腐蚀,可推知溶液pH≤2时,生铁发生析氢腐蚀,故A项正确;pH=4时锥形瓶中气体压强随着反应的进行而逐渐减小,说明发生了吸氧腐蚀,故B项正确;根据压强与时间的关系图知,pH=2的溶液和pH=4的溶液中,变化相同的压强时所用时间不同,
- 10 -
前者比后者时间长,说明吸氧腐蚀速率大于析氢腐蚀速率,故C项错误;两溶液中都发生电化学腐蚀,铁均作负极,负极反应式均为Fe-2e-Fe2+,故D项正确。
二、非选择题(本题包括1小题,共18分)
13.某探究小组用铁钉被腐蚀的快慢实验来研究防止钢铁腐蚀的方法。所用试剂:材质相同的无锈铁钉数个,食盐水、碳酸水、植物油各多量,实验温度为298 K、308 K,每次实验取用铁钉的数量相同。液体体积相同且足量,用大小相同的试管实验。 世纪金榜导学号
(1)请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
实验编号
T/K
试管内取
用液体
实验目的
①
298
食盐水
(Ⅰ)实验①和②探究不同电解质溶液对铁钉腐蚀快慢的影响
(Ⅱ)实验①和____________探究温度对铁钉腐蚀快慢的影响
(Ⅲ)实验①和____________探究铁钉是否接触电解质溶液对铁钉腐蚀快慢的影响
②
③
④
(2)请根据上述实验,判断下列有关钢铁制品防腐的说法正确的是____________(填字母)。
A.在铁门、铁窗表面涂上油漆
B.自行车各部件因有防护涂层或电镀等防腐措施,所以不需要停放在能遮雨的地方
C.家用铁制厨具每次用完后应擦干放置在干燥处
D.把挡水铁闸门与直流电源的正极连接且构成回路,可减少铁闸门的腐蚀速率
【解析】(1)(Ⅰ)探究不同电解质对铁钉腐蚀快慢的影响,因此保证温度不变(仍为298 K),改变电解质(选用碳酸水)。(Ⅱ)探究温度对铁钉腐蚀快慢的影响,因此保证电解质不变(仍为食盐水),改变温度(选308 K)。(Ⅲ)探究铁钉是否接触电解质溶液对铁钉腐蚀快慢的影响,因此保证温度不变(仍为298 K),改变试管内液体(选植物油)。(2)A项涂油漆保护铁门、铁窗,使铁门、铁窗与周围物质隔开,正确;自行车放在遮雨的地方、家用铁制厨具擦干放在干燥处,不易形成原电池,能降低腐蚀速率,B错误,C正确;D项挡水铁闸门应与直流电源的负极相连,使之作电解池的阴极,才能起到保护作用,D错误。
答案:(1)
实验编号
T/K
试管内取
实验目的
- 10 -
用液体
①
(Ⅱ)③
(Ⅲ)④(只要与前面③、④对应即可)
②
298
碳酸水
③
308
食盐水
④
298
植物油
(2)AC
- 10 -
相关文档
- 2020届高考化学一轮复习钠及其重要2021-05-20 18:36:1618页
- 2021版浙江高考选考化学一轮复习教2021-05-20 18:34:3527页
- 2021版浙江高考选考化学一轮复习教2021-05-20 18:34:077页
- 2020-2021学年度中小学语文化学及2021-05-20 18:34:0715页
- 黑龙江省大庆市第十中学2019-20202021-05-20 18:33:376页
- 中考化学专题目8盐和化肥一轮过关2021-05-20 18:29:224页
- 初中化学九年级上册周周清检测内容2021-05-20 18:27:155页
- 化学人教版选修3课件:2-1-2 共价键2021-05-20 18:25:3049页
- 湖南省三湘名校联盟2020-2021学年2021-05-20 18:24:028页
- 2021新高考化学二轮总复习选择题专2021-05-20 18:23:227页