- 319.50 KB
- 2021-04-28 发布
- 1、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 2、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报QQ:3215808601
第二单元 我们周围的空气
课题1 空气(第一课时)
课时目标
1.知道空气的组成
2.认识纯净物和混合物的概念,并能区分这两类物质
3.了解拉瓦锡研究空气成分的实验原理,能初步使用该原理测空气中氧气含量
课堂导学
知识点一 空气是由什么组成
1.拉瓦锡测定空气成分的实验
阅读教材P26,完成以下表格内容。
实验
实验操作
实验现象
实验结论
(1)在密闭容器里加热汞
把少量的汞放在密闭容器里连续加热12天
有部分银白色的液态汞变成红色;空气的体积约减少1/5
空气是由①_______和②_________组成,其中③______约占空气总体积的1/5。该反应的文字表达式为:汞+氧气氧化汞
(2)在另一密闭容器里加热红色粉末
将上述实验得到的红色粉末放在另一密闭容器中加强热
红色粉末逐渐变成银白色;得到的气体体积恰好等于前面实验密闭容器中减少的气体体积
拓展讲解:
反应物 反应条件 生成物
汞 + 氧气氧化汞
(1)文字表达式的含义:“+”念“和”、“与”、或“跟”,“―→”读成“生成”
(2)文字表达式的读法:汞和氧气在点燃的条件下反应生成氧化汞
2.空气中氧气含量的测定
阅读教材P27的实验2-1,并完成实验。根据实验情况填写以下内容。
9
实验装置
实验操作
实验现象
实验结论
点燃红磷,并迅速伸入瓶内
红磷燃烧,④_____________
⑦_____________
_____________
冷却后打开弹簧夹
烧杯的⑤______________,且体积约占瓶容积的⑥______
[实验分析]
集气瓶内水平面上升了约1/5,说明瓶内少了约1/5的气体体积,这是因为红磷(P)与空气中的氧气发生了反应,生成一种叫做五氧化二磷(P2O5)的白色固体,反应的文字表达式为:⑧______________________________________。
[实验注意事项]
(1)该实验对装置的气密性要求较高,实验前应先检查⑨______________。
(2)在瓶内预留了些水,其作用是吸收五氧化二磷,减少⑩____________。
(3)为充分消耗瓶内氧气,红磷的用量要⑪__________。
(4)燃烧匙伸进瓶内后应迅速塞紧瓶塞,防止瓶内气体受热膨胀往外逸散,导致瓶内气体减少偏多,测定结果会偏大。
(5)为防止瓶内气体受热膨胀带来的影响,需待装置冷却后再打开弹簧夹。
(6)实验药品的选择:
必须符合两个条件:在空气中易燃烧、燃烧后生成物是⑫________。
[拓展推理]
通过该实验还可推知剩余气体的性质有:⑬__________________________________。
典例解析
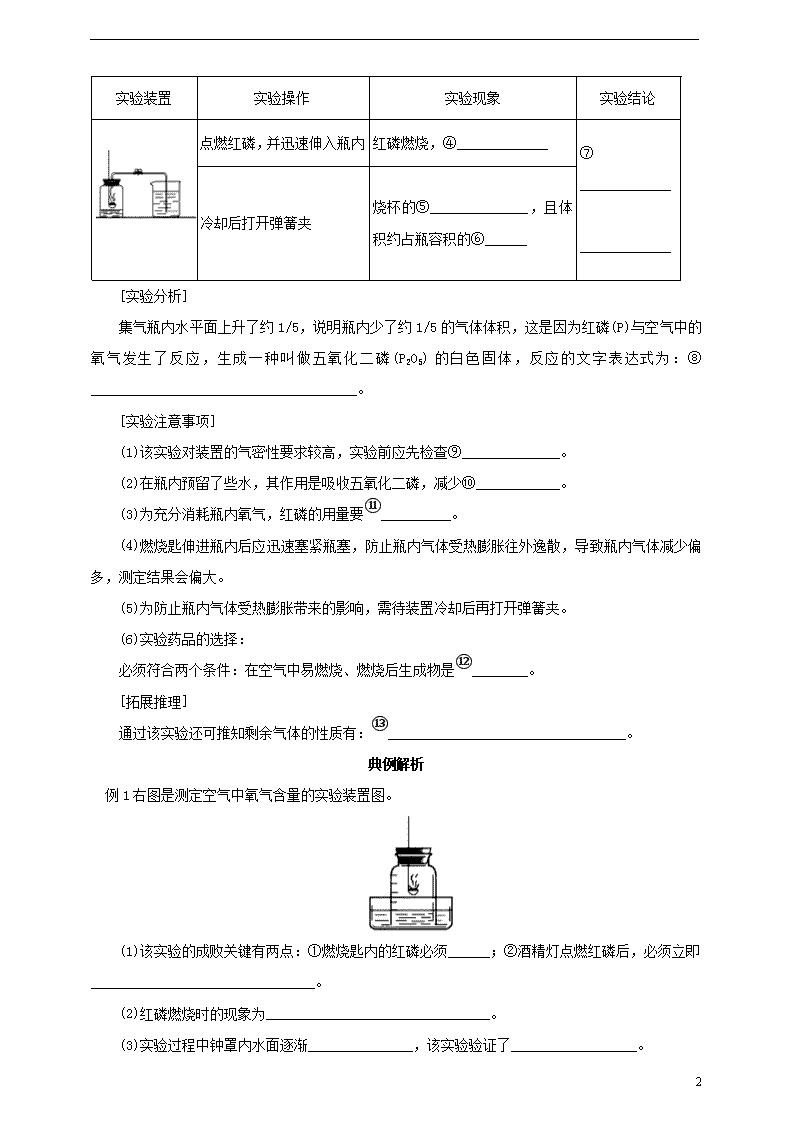
例1右图是测定空气中氧气含量的实验装置图。
(1)该实验的成败关键有两点:①燃烧匙内的红磷必须______;②酒精灯点燃红磷后,必须立即________________________________。
(2)红磷燃烧时的现象为________________________________。
(3)实验过程中钟罩内水面逐渐_______________,该实验验证了__________________。
9
(4)若实验中红磷的量太少,测得氧气的体积分数会______;若钟罩的气密性不好,测得氧气的体积分数会______。
(5)若实验结束,钟罩中水位上升不到预期位置,则实验失败的原因可能是:______(写出一点)。
解析:(1)该实验的成败关键有两点:①燃烧匙内的红磷必须足量或过量;②酒精灯点燃红磷后,必须立即塞紧瓶塞;(2)红磷燃烧时的现象为黄色火焰,产生大量白烟,放出热量;(3)实验过程中,钟罩内水面逐渐上升,该实验验证了氧气约占空气体积的五分之一;(4)若实验中红磷的量太少,氧气消耗不尽,测得氧气的体积分数会偏小,若钟罩的气密性不好,气体膨胀时跑出的是氮气,冷却时进入的是空气,测得氧气的体积分数会偏小;(5)若实验结束,钟罩中水位上升不到预期位置,则实验失败的原因可能是装置漏气或红磷量不足。
答案:(1)足量或过量、塞紧瓶塞(2)黄色火焰,产生大量白烟,放出热量(3)上升,氧气约占空气体积的五分之一(4)偏小、偏小(5)装置漏气或红磷量不足
变式练习
1. 如图装置是用来测定空气中氧气的含量。下列对该实验的认识正确的是( )
A. 红磷燃烧产生大量白色烟雾
B. 燃烧匙中的红磷可以换成蜡烛
C. 红磷刚燃烧完就立即打开弹簧夹,会导致实验结果偏小
D. 红磷的量不足会导致进入集气瓶中水的体积大于1/5
2. 小明学习了空气中氧气含量的测定实验后,提出了改进方法(如右图所示),你认为改进后的优点是______________________________________________________(任写两点)。
3.空气的组成
阅读教材P27,背熟空气成分后进行默写。
空气成分
氮气(N2)
O2
稀有气体
CO2
其他气体和杂质
体积分数
⑭
⑮
⑯
⑰
⑱
特点
相对稳定
成分可变
拓展讲解:空气中的氮气、氧气、稀有气体可直接从空气中分离得到,而CO2
9
、其他气体和杂质因其含量太少,无法从空气中分离得到。
4.混合物和纯净物
阅读教材P27,找到混合物和纯净物的概念,并进行初步认识。
类型比较
混合物
纯净物
概念
由⑲_______________混合而成。
只由⑳________________组成。
特征
①没有固定的组成和性质
②不能用化学符号表示
③各成分保持它们各自的性质
有固定的组成与性质,可以用化学符号表示。
举例
空气、稀有气体 等
氧气、氮气等
联系
纯净物混合物
典例解析
例2下列物质属于混合物的是( )
A.冰水混合物 B.氧气 C.澄清的矿泉水 D.氮气
解析:纯净物只含有一种物质,混合物由不同种的物质组成。冰水混合物,只有水一种物质,澄清的矿泉水中除水外还有一些物质溶解在水中。
答案:C
知识拓展:
1.生活中常见的混合物有:空气、稀有气体、粮食、合金(生铁、钢、18K黄金等)、溶液(矿泉水、自来水等)、饮料类、矿物类(大理石)等;
2.常见的纯净物有:水(纯净水、蒸馏水、冰水)、金属(铁、铜、铝、24K黄金等)、氧气、二氧化碳、蔗糖等。
变式练习
3.下列物质中,属于纯净物的是( )
A.空气 B.五氧化二磷 C.湖水 D.米酒
4. 下列各组物质中,前者属于纯净物,后者属于混合物的是( )
A. 二氧化碳,澄清石灰水 B. 冰水混合物,五氧化二磷
C. 矿泉水, 河水 D. 净化后的空气,受污染的空气
课堂小结
一、空气是由什么组成
1.拉瓦锡测定空气的成分的实验得出空气是由______和______组成的结论
9
2.空气里氧气含量的测定
(1)实验原理;(2)实验现象;(3)实验结论,拓展推理剩余气体的性质
(4)实验注意事项:①导致测定值偏小的原因;②导致测定值偏大的可能原因
(5)实验药品的选择
3.空气的组成:空气的成分及其体积分数
4.混合物和纯净物
课时达标
1.下列现象的产生,与空气中的水蒸气无关的是( )
A.酥脆的饼干放置在空气中变软
B.夏天从冰箱取出的冰糕冒“白气”
C.冬季的早晨看到窗户的玻璃上有“冰花”
D.进入久未开启的菜窖或干涸深井使人感到气闷、头昏
2.下列是生产、生活中常用的物质,其中不属于混合物的是( )
A.冰红茶 B.牛奶 C.洗洁精 D.氧气
3.右图所示是一个具有刻度和活塞可滑动的玻璃容器,其中有空气和足量的白磷,将它放在盛有沸水的烧杯上方,进行试验。请完成下列问题。
(1)实验现象:白磷着火燃烧,活塞先右移,后左移,最后停在刻度约为________的位置上。
(2)白磷燃烧的文字表达式为_________________________________________________。
(3)实验结论:空气的成分按体积计算,氧气约占__________。
课后作业
A 双基过关
1. 空气成分中不包含下列哪种物质?( )。
A. 氧气 B. 氮气 C. 稀有气体 D. 氢气
2. 人的生存离不开空气。下图为空气成分示意图,其中R指的是( )。
9
A. 氮气 B. 氧气
C. 稀有气体 D. 二氧化碳
3. 下列有关空气的说法正确的是( )。
A. 通常情况下,空气中氧气、氮气的体积比约为1∶4
B. 空气中氮气的质量分数为78%
C. 空气中二氧化碳的体积只占0.03%,因此它的作用很小
D. 空气中含量最少的是稀有气体
4. 下列各组物质中,前者是纯净物,后者是混合物的是( )。
A. 氢氧化钠 稀盐酸
B. 碘酒 红磷
C. 空气 氧气
D. 海水 石灰石(主要成分为碳酸钙)
5. 在课本测定空气中氧气含量的实验中,集气瓶内剩余的气体主要是氮气,体积约为集气瓶空气体积的五分之四,下列结论与此实验事实无关的是( )。
A. 氮气不支持燃烧 B. 氮气不易溶于水
C. 氮气的熔点是-209.9℃ D. 空气中氮气和氧气的体积比约为4∶1
6. 下列物质中,属于纯净物的是( )。
7. 按下图组装仪器,关闭止水夹,通电使红磷燃烧。请回答下列问题:
9
(1)燃烧的现象是_________________________,反应的文字表达式为______________________________。
(2)红磷燃烧一段时间后,自动熄灭了,你认为原因是___________________。
(3)冷却后,松开止水夹,你观察到的现象为___________________________________________________。
(4)小华同学用炭替代红磷,完成上述实验,发现集气瓶内并没有吸入水,其原因是_______________________________________________________________________________。
(5)用此实验方法测定空气中氧气的含量,其优点是___________________________。
8. 填表,列举一些常见的纯净物和混合物,每类只列举一种。
状态
类别
固态
液态
气态
纯净物
混合物
B能力提高
9. 装在某容器中的空气经测定其中氮气的体积在相同条件下为10L,则该容器的容积为( )。
A. 10L B. 15L C. 12.5L D. 18L
10. 为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为40mL的试管作反应容器,将过量的白磷放入试管,用橡皮塞塞紧试管,通过导管与实际容积为60mL且润滑性很好的针筒注射器组成如下图的实验装置。假设此实验能够按照小华的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题:
9
(1)实验前,打开弹簧夹,将注射器活塞前沿从20mL 刻度处推至15mL刻度处,然后松开手,若活塞仍能返回至20mL刻度处,则说明:_______________________________;
(2)若先夹紧弹簧夹,用酒精灯加热白磷,燃烧结束,等试管冷却后再松开弹簧夹,可观察到的现象为_____________________________________________;
(3)若不使用弹簧夹,用酒精灯加热白磷,充分反应直至燃烧结束,试管冷却后可观察到的现象为________________________________________________;
(4)若按小华的设想进行实验,实际可能遇到诸多问题而发生危险,造成实验失败,例如:__________________________________________________________。
参考答案
课堂导练
①氮气 ②氧气 ③氧气 ④产生大量白烟并放热 ⑤水进入集气瓶 ⑥1/5 ⑦氧气约占空气体积的1/5 ⑧磷+氧气五氧化二磷 ⑨ 装置的气密性 ⑩环境污染 ⑪过量 ⑫固体 ⑬
9
化学性质不活泼,不能溶于水 ⑭78% ⑮21% ⑯0.94% ⑰0.03% ⑱0.03% ⑲两种或两种以上的物质 ⑳一种物质
变式训练
1.C 2.方便 减少误差3. B 4. A
课堂小结
氧气 氮气
课时达标
1.D 2.D 3. 8 磷+氧气五氧化二磷 1/5
课后作业
A 双基过关
1. D 2. B 3. A 4. A 5. C 6. C
7. (1)产生大量白烟并放出热量
磷+氧气 五氧化二磷
(2)瓶内的氧气消耗完了
(3)烧杯中水倒流入集气瓶,约占集气瓶体积的1/5
(4)碳燃烧生成二氧化碳气体不能形成压强差
(5)不会污染空气
8. 铜 水 氧气,生铁 糖水 空气
B 能力提高
9. C
10. (1)装置气密性良好
(2)白磷燃烧,产生白烟,活塞前沿约在12mL的刻度线上
(3)白磷燃烧,产生白烟,活塞先向右移动,最终稳定在约8mL的刻度线上
(4)橡胶塞弹出、试管爆裂、注射器活塞弹出等
9
相关文档
- 2019九年级化学上册 第二章 身边的2021-04-27 23:45:074页
- 新课标RJ2020中考化学复习方案主题2021-04-27 20:57:0823页
- 安徽专版2020中考化学复习方案主题2021-04-27 16:36:2763页
- 河北专版2020中考化学复习方案主题2021-04-25 20:09:0947页
- 北京专版2020中考化学复习方案主题2021-04-25 18:01:208页
- 2014中考化学专题复习训练二 身边2021-04-22 21:02:215页
- 中考化学身边的化学物质一轮专题目2021-04-22 20:15:507页
- 包头专版2020中考化学复习方案主题2021-04-22 18:50:328页
- 呼和浩特专版2020中考化学复习方案2021-04-21 23:00:0616页
- 2014中考化学专题复习训练二 身边2021-04-21 01:20:473页