- 246.34 KB
- 2023-04-13 发布
专项(六)
酸碱盐之间的共存、鉴别及转化
主题一 身边的化学物质
考点突破
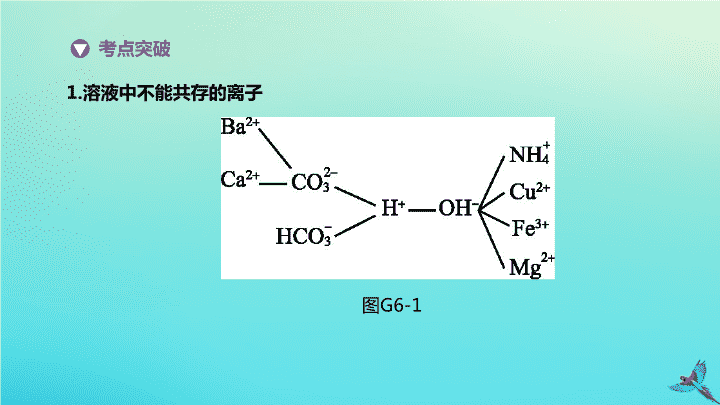
1.
溶液中不能共存的离子
图
G6-1
2.
酸碱盐之间的转化
酸碱盐之间反应后均有盐生成
,
以常见盐为生成物
,
写出对应的反应物
(
合理即可
)
。
盐
酸
+
碱
酸
+
盐
碱
+
盐
盐
+
盐
NaCl
_______________
_________________
_____________________
_________________
Na
2
CO
3
CaCl
2
________________
_________________
_____________________
CaCO
3
_____________________
_________________
HCl+NaOH
HCl+Na
2
CO
3
NaOH+CuCl
2
CaCl
2
+Na
2
CO
3
HCl+Ca(OH)
2
HCl+CaCO
3
Ca(OH)
2
+NH
4
Cl
Ca(OH)
2
+Na
2
CO
3
CaCl
2
+Na
2
CO
3
(续表)
盐
酸
+
碱
酸
+
盐
碱
+
盐
盐
+
盐
BaCO
3
_____________________
_________________
CuSO
4
____________
_____________
AgCl
_________________
BaSO
4
____________
_____________
_________________
_____________________
_________________
Ba(OH)
2
+Na
2
CO
3
BaCl
2
+Na
2
CO
3
H
2
SO
4
+
AgNO
3
+NaCl
H
2
SO
4
+
H
2
SO
4
+BaCl
2
Ba(OH)
2
+Na
2
SO
4
BaCl
2
+Na
2
SO
4
Cu(OH)
2
Ba(OH)
2
3.
反应后成分分析
(1)
结论及依据
①
生成物一定有
,
反应物不可能同时有。例如
,
氢氧化钠与盐酸反应
,
反应后物质中一定有氯化钠
,
可能有氢氧化钠或盐酸
,
但氢氧化钠和盐酸不能同时存在。
②
溶液颜色限定
,
无色溶液中一定不含铁离子、铜离子、亚铁离子等。
(2)
反应程度分析
——
酸碱盐优先反应
Ⅰ.
酸碱盐优先反应的两种情况
分类
举例
分析及方程式
①H
+
优先与
OH
-
发生反应
(
或
OH
-
优先与
H
+
发生反应
)
将
NaOH
溶液逐滴加入到
CuSO
4
和
H
2
SO
4
的混合溶液中
现象
:
_____________________________________________
____________
先
:
________________________________________
后
:
_____________________________________________
刚开始时无明显现象
,
过一会儿有蓝色絮状
2NaOH+H
2
SO
4
Na
2
SO
4
+2H
2
O
2NaOH+CuSO
4
Na
2
SO
4
+Cu(OH)
2
↓
沉淀生成
(续表)
分类
举例
分析及方程式
①H
+
优先与
OH
-
发生
反应
(
或
OH
-
优先与
H
+
发生反应
)
将
盐酸逐滴加入到
NaOH
和
Na
2
CO
3
的混合溶液中
现象
:
________________________________________
_______
先
:
________________________________
后
:
__________________________________________
②
碳酸盐优先与
H
+
发生反应
将
Na
2
CO
3
溶液逐滴加入到
CaCl
2
和稀盐酸的混合溶液中
现象
:
________________________________________
_________________________
先
:
__________________________________________
后
:
________________________________________
刚开始时无明显现象
,
过一会儿有气泡
NaOH+HCl NaCl+H
2
O
Na
2
CO
3
+2HCl 2NaCl+H
2
O+CO
2
↑
刚开始时有气泡产生
,
过一会儿无气泡
Na
2
CO
3
+2HCl 2NaCl+H
2
O+CO
2
↑
Na
2
CO
3
+CaCl
2
CaCO
3
↓
+2NaCl
冒出后有白色沉淀生成
产生
Ⅱ.
将稀硫酸加入到
NaOH
和
BaCl
2
的混合溶液中
,
由于
H
+
与
OH
-
和
Ba
2+
与
S
均只发生一个化学反应
,
所以不存在先后顺序
,
生成沉淀和酸碱中和是两个独立的过程
,
反应开始
,
两个反应同时发生
,
可观察到
,
该过程发生反应的化学方程式为
、
、
。
刚开始时就有白色沉淀生成
H
2
SO
4
+2NaOH Na
2
SO
4
+2H
2
O
Na
2
SO
4
+BaCl
2
BaSO
4
↓
+2NaCl
H
2
SO
4
+BaCl
2
BaSO
4
↓
+2HCl