- 872.00 KB
- 2021-05-27 发布
- 1、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 2、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报QQ:3215808601
初级药师考试辅导 基础知识
第 1页
药物分析
考试大纲的三个要求层次:
了解
掌握
熟练掌握
药品质量标准
医学课程购买联系 QQ:2939831027 其他联系购买的均为倒卖,后续课程更新务必添加 QQ
考试要求:
细目 要点
1.概述
(1)药品质量控制目的与质量管理的意义
(2)全面控制药品质量
2.药品质量标准
(1)药品质量标准
(2)中国药典
(3)制定药品质量标准的基本原则与依据
3.常用的分析方法
(1)定性方法:化学鉴别法、光谱鉴别法、色谱鉴别法
(2)定量方法:滴定法、分光光度法、色谱法
一、概述
(一)药品质量控制的目的、质量管理的意义
保证用药的安全、合理和有效
常见的质量管理文件:《药品非临床研究质量管理规范》(GLP)、《药品经营质量管理规范》(GSP)、
《药品生产质量管理规范》(GMP)《药品临床试验管理规范》(GCP)。
(二)全面质量控制:
研制、生产、供应、临床使用
静态分析 综合评价、动态分析
二、药品质量标准
(一)药品质量标准
是国家对药品质量、规格及检验方法所做的技术规定,是药品生产、供应、使用、检验和药政管理部
门共同遵循的法定依据。
国内药品标准:《中国药典》(Ch.P.)、药品标准;
国外药品标准:美国药典(USP)、美国国家处方集(NF)、英国药典(BP)、日本药局方(JP)、欧
洲药典(Ph.Eup)和国际药典(Ph.Int)。
(掌握各自的简称)
(二)《中国药典》
1.历史沿革:
建国之后至今共出了十版:
1953、1963、1977、1985、1990、1995、2000、2005、2010、2015 年版
1963:开始分一、二两部。
2005:开始分三部,第三部收载生物制品。
2015:开始分四部。
2.基本结构和主要内容
初级药师考试辅导 基础知识
第 2页
《中国药典》由一部、二部、三部、四部组成,首次将通则、药用辅料单独作为《中国药典》四部。
凡例(重点掌握一些概念和解释)
凡例是为解释和使用中国药典,正确进行质量检验提供的指导原则。
关于检验方法和限度的规定
检验方法:《中国药典》规定的按药典,采用其他方法的要与药典方法对比。仲裁以《中国药典》方
法为准。
关于标准品和对照品的规定
标准品、对照品系指用于鉴别、检查、含量测定的标准物质,由国务院药品监督管理部门指定的单位
制备、标定和供应。
标准品:用于生物检定、抗生素或生化药品中含量或效价测定的标准物质,按效价单位(或μg)计,
以国家标准品标定。
对照品指用于检测时,按干燥品(或无水物)计算后使用的标准物质。
举例:对照品 10g,含水量为 10%,按干燥品计算的对照品为 9g。
考点:混淆标准品、对照品的概念
标准品按效价,对照品要干燥
关于精确度的规定
“精密称定”指称取重量应准确至所取重量的千分之一;
例:0.2g 精密称定,0.2XXXg
“称定”指称取重量应准确至所取重量的百分之一;
“精密量取”指量取体积的准确度应符合国家标准中对该体积移液管的精密度要求。
取用量为“约”若干时,指取用量不得超过规定量的十分之一。
试验中供试品与试药等“称重”或“量取”的量,均以阿拉伯数码表示,其精确度可根据数值的有效
数位来确定。(小数点后多一位)
称取“0.1g”,系指称取重量可为 0.06~0.14g;
称取“2g”,指称取重量可为 1.5~2.5g;
称取“2.0g”,指称取重量可为 1.95~2.05g;
称取“2.O0g”,指称取重量可为 1.995~2.O05g。
“空白试验”系指在不加供试品或以等量溶剂替代供试液的情况下,按同法操作所得的结果;
含量测定中的“并将滴定的结果用空白试验校正”,是指按供试品消耗滴定液的量 (ml)与空白试验
中所耗滴定液的量(ml)之差进行计算。
试液、试药、指示剂——符合相关规定
计量
1→10 符号:固体溶质 1.0g 或液体溶质 1.0ml 加溶剂使成 10ml 的溶液;
初级药师考试辅导 基础知识
第 3页
正文
按顺序可分别列有:名称、有机药物的结构式、分子式与分子量、来源或有机药物的化学名称、含量
或效价的规定、处方、制法、性状、鉴别、检查、含量或效价测定、类别、规格、贮藏及制剂等。
通则
制剂通则、鉴定方法、标准物质、试剂试药和指导原则。
(三)制定药品质量标准的基本原则与依据
基本原则:
坚持质量第一,充分体现“安全有效、技术先进、 标准合理、方法规范”的原则。
①检测项目和限度——针对性、合理性
②检测手段选用——可行性、先进性
三、常用的分析方法(非常重要)
1.常用的定性方法
(1)化学鉴别法
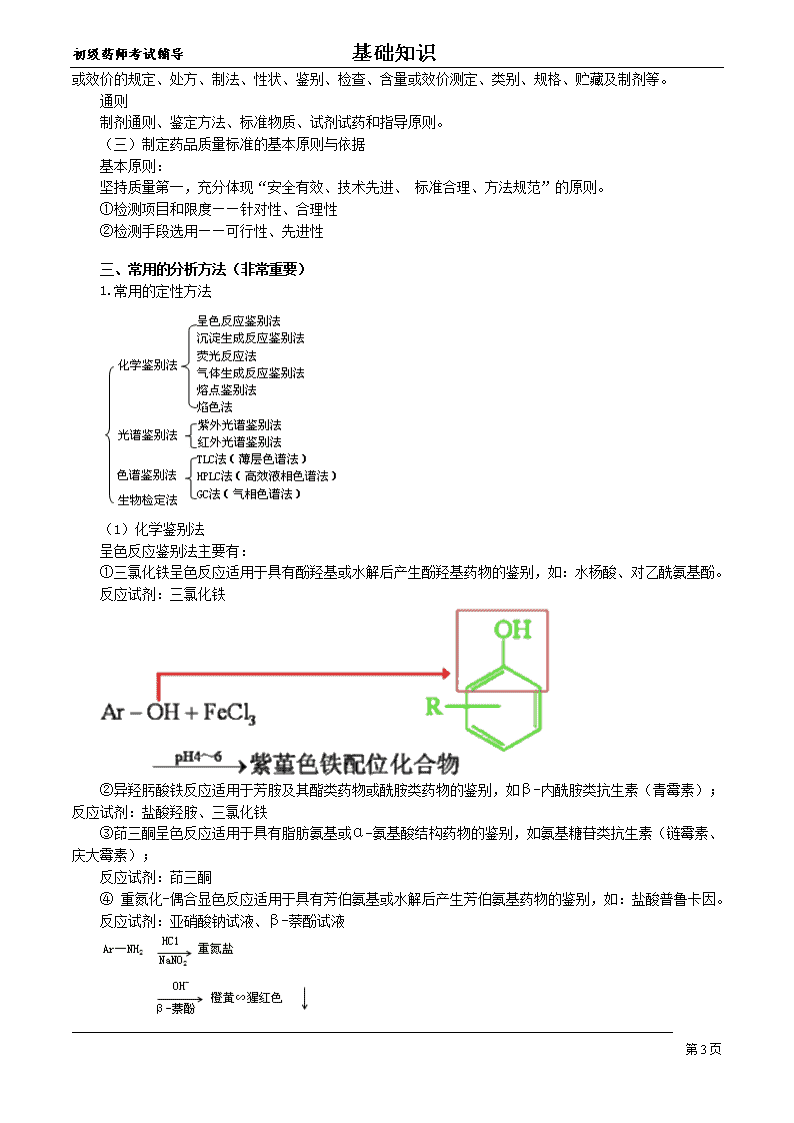
呈色反应鉴别法主要有:
①三氯化铁呈色反应适用于具有酚羟基或水解后产生酚羟基药物的鉴别,如:水杨酸、对乙酰氨基酚。
反应试剂:三氯化铁
②异羟肟酸铁反应适用于芳胺及其酯类药物或酰胺类药物的鉴别,如β-内酰胺类抗生素(青霉素);
反应试剂:盐酸羟胺、三氯化铁
③茚三酮呈色反应适用于具有脂肪氨基或α-氨基酸结构药物的鉴别,如氨基糖苷类抗生素(链霉素、
庆大霉素);
反应试剂:茚三酮
④ 重氮化-偶合显色反应适用于具有芳伯氨基或水解后产生芳伯氨基药物的鉴别,如:盐酸普鲁卡因。
反应试剂:亚硝酸钠试液、β-萘酚试液
初级药师考试辅导 基础知识
第 4页
⑤氧化还原显色反应适用于具有还原基团药物的鉴别,如:维生素 C。
沉淀生成反应鉴别法主要有:
①与重金属离子的沉淀反应,如与银盐、铜盐的反应,如:巴比妥类药物;
②与硫氰化铬铵的沉淀反应;
③其他沉淀反应。
荧光反应法主要有三种情况:
①药物本身在可见光(或紫外光)下发射荧光;
②药物溶液加硫酸使呈酸性后,在可见或紫外光下发射荧光;
③药物与某些试剂如溴、间苯二酚、衍生化试剂等反应,于可见光下发射荧光。
气体生成反应鉴别法:利用药物与某些试剂在一定条件下反应可生成特征气体的原理,通过对此种气
体的鉴别来确定药物种类的方法。主要有:
①胺类、酰脲类、酰胺类药物经强碱处理后,产生氨气;(含 N 的药物产生氨气)
②含硫的药物经强酸处理后,产生 H2S 气体;
③含碘的有机药物加热,生成紫色碘蒸气;
④含醋酸酯、乙酰胺类药物水解后,加乙醇,产生醋酸乙酯的香味。(含酯键药物产生香味)
(2)光谱鉴别法:主要包括紫外光谱鉴别法和红外光谱鉴别法。
紫外光谱鉴别法(UV):
200nm~400nm 为紫外光区;——共轭双键
400nm~760nm 为可见光区;——有色溶液
鉴别方法:
①测定最大吸收波长(λmax),或同时测定最小吸收波长(λmin);
②规定一定浓度的供试液在最大吸收波长处的吸收度;
③规定吸收波长和吸收系数法;
④规定吸收波长和吸收度比值法;
⑤经化学处理后测定其反应产物的吸收光谱特性。
初级药师考试辅导 基础知识
第 5页
红外光谱法:
采用标准图谱对照法
(3)色谱鉴别法:包括 TLC 法、HPLC 法和 GC 法。
TLC 法一般采用对照品(标准品)比较法,要求供试品斑点的比移值(Rf)与对照品的一致。
HPLC 法和 GC 法一般采用对照品(标准品)比较法,要求供试品溶液中药物色谱峰的保留时间(tR)与
对照品的一致。
供试品 对照品
图 用已知纯物质与未知样品对照比较进行性分析
1~9—未知物的色谱峰 a—甲醇峰 b—乙醇峰
c—正丙醇峰 d—正丁醇峰 e—正戊醇峰
2.定量分析方法
(1)滴定法:
方法:将已知浓度的滴定液滴加到待测药物的溶液中,直到所加滴定液与被测药物按化学计量反应完
全为止,根据滴定液的浓度与消耗滴定液的体积计算被测药物的含量。
初级药师考试辅导 基础知识
第 6页
举例:NaOH+HCl——H2O+NaCl
aA+bB→cC+dD
计算方法:
①直接按计量关系计算
②通过滴定度计算
滴定度为每 1ml 某摩尔浓度的滴定液相当于被测物质的重量(mg)。
含量计算:
直接滴定法:
剩余滴定法:
重点:滴定液、指示剂
滴定液:装在滴定管里用来和药物反应的试液。
指示剂:用来指示反应终点的试剂。
补充:常见滴定方法:
①亚硝酸钠法(氧化还原法的一种):又称重氮化法,是以亚硝酸钠为滴定液测定具有芳伯氨基(普
鲁卡因、磺胺类)或经适当化学反应(如水解、还原等)后产生芳伯氨基(如对乙酰氨基酚、氯霉素等)
的药物的含量。
指示终点的方法有三种:
a.外指示剂法:以碘化钾淀粉糊或溶液为外指示剂。
b.内指示剂法:常用的指示剂有橙黄Ⅳ-亚甲蓝、中性红等。
c.永停滴定法:本法是利用永停滴定仪指示终点的方法,为我国药典所采用。
②非水滴定法:适于酸碱性不太强的有机碱或有机酸类药物的含量测定。有机碱的含量测定,常以冰
醋酸为溶剂,高氯酸为滴定液,结晶紫为指示剂。如:生物碱类药物的含量测定;
③沉淀滴定法:主要指银量法,即以硝酸银为滴定液测定含卤素离子药物的含量。如巴比妥类药物的
测定;
④酸碱滴定法:适用于酸、碱药物的含量测定。常用滴定液:盐酸滴定液、氢氧化钠滴定液。指示剂:
甲基红、酚酞。如:芳酸类药物的含量测定。
(2)光谱分析法
①紫外-可见分光光度法:定量依据是 Lambert-Beer 定律:
A=-lgT=-lgl/l0=ECL
式中的 E 为吸收系数,有两种表达方式:摩尔吸收系数(ε)和百分吸收系数( )。当被测物浓
初级药师考试辅导 基础知识
第 7页
度(C)以 mol/L 为单位时,E 为摩尔吸收系数;当 C 的单位为 1g/1OOml 时,E 为百分吸收系数。ε与
的关系为:ε=M/10× 。
紫外-可见分光光度法中常用的定量方法有:
A.对照品比较法:
B.吸收系数法:
注意:测定时,要求供试品溶液的 A 应在 0.3~0.7。
C.计算分光光度法
双波长、导数光谱法。用于复杂样品的分析。
②荧光分光光度法:物质在低浓度范围内的荧光强度与溶液中该物质的浓度成正比。
答题技巧:通过判断公式中有无吸收系数,确定是何种方法
(3)色谱分析法:是一种分离分析方法,该法先将混合物中各组分分离,然后逐一检测。
高效液相色谱法(HPLC)、气相色谱法(GC)。
高效液相色谱法:以液体为流动相的色谱法。
分类:
正相 HPLC 反相 HPLC
固定相 硅胶 十八烷基硅烷键合硅胶
流动相 有机溶剂混合液(烷烃为底剂,加入适量的极性溶剂组成)
甲醇-水
乙腈-水
洗脱顺序 极性小的组分先流出 极性大的组分先流出
应用 极性和中等极性化合物 非极性、弱极性及中等极性化合物
仪器:
流动相储液瓶、输液泵、进样器、色谱柱、检测器、数据处理系统。
初级药师考试辅导 基础知识
第 8页
常见检测器:紫外检测器、二极管阵列检测器、蒸发光散射检测器、质谱检测器。
气相色谱法:以气体为流动相的色谱法。
分类:填充柱、毛细管柱。
仪器:气源系统、进样系统、色谱柱、检测系统、数据处理系统
常用检测器:火焰离子化检测器(FID)
初级药师考试辅导 基础知识
第 9页
HPLC、GC 法的系统适应性试验:
图 色谱图及色谱峰参数示意图
①理论塔板数:n=16(tR/W)2 =5.54 (tR/Wh/2 )2
②分离度:R =2(tR2-tR1) /(W1+W2)
图 不同分离度时色谱峰分离的程度
定量分析时分离度的要求:分离度大于 1.5
③重复性:标准偏差不大于 2.0%
④拖尾因子:T
初级药师考试辅导 基础知识
第 10页
常用定量方法:
①内标法加校正因子测定供试品中主成分含量
校正因子(f)= 含量(CX)=
②外标法测定供试品中主成分含量:分为标准曲线法和外标一点法,外标一点法的计算公式为:
(4)生物检定法:有肝素生物检定法、胰岛素生物检定法、洋地黄生物检定法等。
试题分析
下列关于 2015 版中国药典组成的说法,正确的是
A.中国药典由一部、二部组成
B.中国药典由一部、二部、三部组成
C.中国药典由一部、二部、三部、四部组成
D.中国药典由一部、二部、三部及其增补本组成
E.中国药典由一部、二部、三部及《附录》
『正确答案』C
试题分析
在药品含量测定中,取对照品约 10 ㎎,精确至
A.0.1g
B.0.01g
C.1mg
D.0.1mg
E.0.01mg
『正确答案』C
试题分析
初级药师考试辅导 基础知识
第 11页
A.BP B.Ch.P
C.JP D.Ph.E E.USP
1.美国药典的英文缩写是
2.中国药典的英文缩写是
3.英国药典的英文缩写是
4.日本药局方的英文缩写是
『正确答案』E、B、A、C
含芳香伯氨基药物的鉴别反应是
A.与硝酸银反应
B.重氮化-偶合反应
C.与三氯化铁反应
D.铜吡啶反应
E.维他利反应
『正确答案』B
『答案解析』考察常用的鉴别反应
药品质量控制
考试要求:
细
目
药典
通
则
(1)药检的任务和技术要求
(2)医院内部药品流通环节的质量监控质量跟踪报告制度
(3)药检序程:取样、鉴别、检查、含量测定、留样、写出检验报告
(4)药品质量控制的常见通用项目:重量差异或装量差异、含量、含量均匀度、释放度、溶出度、融变时
限、崩解时限、微生物限度、无菌、不溶性微粒的法定检查方法及结果判定
片剂、胶囊剂
各种片剂的特点和质量要求(口腔贴片、咀嚼片、分散片、泡腾片、阴道片、肠溶片、
速释、缓释-控释片、口腔崩解片)
注射剂和滴眼剂
(1)注射剂的装量、注射用无菌粉末的装量差异的检查方法
(2)可见异物检查方法
(3)热原或细菌内毒素检查的临床意义和方法
(4)静脉滴注用注射液、注射用混悬液、注射用无菌粉末及附加剂的质量要求
(5)检漏方法
(6)滴眼剂的装量、可见异物、混悬型滴眼剂粒度与沉降体积比、渗透压摩尔浓度、
无菌检查的意义
栓剂 质量检查项目,融变时限检查的意义
软膏剂、眼膏剂
(1)粒度检查的意义
(2)对大面积烧伤、严重损伤皮肤时用软膏,用于伤口、眼部手术用眼膏剂应做无
菌检查
气(粉)雾剂及喷雾剂 各型气雾剂检查的项目如每瓶总揿次、每瓶总喷次、每揿主药含量、每喷喷量、雾滴
初级药师考试辅导 基础知识
第 12页
(粒)分布、喷射速率、喷出总量的含义和意义
颗粒剂 粒度、干燥失重、溶化性检查的含义和意义
滴耳剂、滴鼻剂、洗剂、搽
剂、凝胶剂
装量、微生物限度检查的意义
透皮贴剂 释放度检查的含义和意义
混悬剂 质量检查的项目和意义
膜剂 质量检查的项目和意义
乳剂 质量检查的项目和意义
复方制剂分析 复方制剂分析的特点及要求
重点:1.药品质量控制的常见通用项目
2.片剂的质量要求
一、通则
1.药检任务:
药检工作是药品监督管理和药品质量控制的重要组成部分,是运用物理学、化学、物理化学和生物学
的方法,对各种药物及其制剂进行质量检验,判断其质量是否符合药品质量标准的规定。药检工作不仅仅
包括常规的检验,还应包括工艺流程、反应历程、生物体内代谢过程等方面的监测。药品检验可分为:抽
检、委托检验、复核检验、注册检验、仲裁检验和进出口检验。
2.药品检验程序
(1)取样:
取样应具有科学性、真实性和代表性。取样的基本原则应该是均匀,合理。
①样品总件数 X≤3 时,每件取样;
②样品总件数 3<X≤300 时,按 的取样量进行随机取样;
③样品总件数 X>300 时,按 取样量随机取样。
取样后可按等量混合后检验。
(2)药品的鉴别:依据药物的化学结构和理化性质进行某些化学反应,测定某些理化常数或光谱特性,
来判断药物及其制剂的真伪。
(3)药物的检查:药典中检查项下包括有效性、均一性、纯度要求与安全性四个方面;药物的纯度控
制主要是通过对药物中存在的杂质检查来进行的。
(4)药物的含量测定:测定药物中主要有效成分的含量。化学分析、理化分析。
(5)留样:留样数量不得少于一次全项检验用量。留样检品保存一年,进口检品保存一年,中药材保
存半年,医院制剂保存 3 个月。
(6)检验记录与报告:检验记录必须真实、完整、科学。
3.药品质量控制的常见通用项目
(1)重量差异检查:重量差异是指按规定称量方法测得每片的重量与平均片重之间的差异程度。
初级药师考试辅导 基础知识
第 13页
检查意义:在片剂生产中,由于颗粒的均匀度、流动性及生产设备等原因可使片剂重量产生差异影响
临床用药,所以应规定该项检查。(片重差异影响临床用药)
检查方法:取药片 20 片,精密称定总重量,求得平均片重,再分别精密称定每片的重量,计算每片片
重与平均片重差异的百分率。
要求:
表 片剂重量差异的限度
平均重量 重量差异限度
0.30g 以下 ±7.5%
0.30g 或 0.30g 以上 ±5%
结果判断:超出重量差异限度的药片不得多于 2 片,并不得有一片超出限度 1 倍。
(2)装量、装量差异检查
液体药物检查装量,注射用无菌粉末检查装量差异
(3)含量均匀度检查法:含量均匀度是指小剂量口服固体制剂、胶囊剂、膜剂或注射用无菌粉末中的
每片(个)含量符合标示量的程度。
检查意义:当片剂中药物的含量较低时,如每片含几毫克或零点几毫克,药物在颗粒中的均匀度较难
控制,仅靠重量差异检查已不能完全反映药物含量的均匀程度,所以需做含量均匀度检查。
凡检查含量均匀度的制剂不再检查重(装)量差异。
(4)崩解时限:指固体制剂在规定的介质中,以规定的方法进行检查全部崩解溶散或成碎粒并通过筛
网所需时间的限度。
检查意义:固体制剂经口服后在胃肠道中先崩解,药物才能被释放、吸收。如果不能崩解,药物就无
法吸收,也就起不到治病的目的。所以固体制剂需要进行崩解时限检查。
检查方法:崩解仪。
要求: 固体制剂崩解时限
剂型 崩解介质 崩解时间(min) 温度(℃)
片剂 水 15 37±1
糖衣片、薄膜衣片或浸膏片 盐酸溶液(9→1000) 60/30 37±1
肠溶片
盐酸溶液(9→1000) 120 37±1
磷酸盐缓冲液(pH6.8) 60
泡腾片 水 5 15~25
凡规定检查溶出度、释放度或融变时限或分散均匀性的制剂,不再进行崩解时限检查。
(5)溶出度:指药物从片剂或胶囊剂等固体制剂在规定溶剂中溶出的速度和程度。
检查意义:固体制剂经口服后在胃肠道中需崩解、溶解、吸收等过程,才能产生药效。崩解是药物溶
出的前提,但由于药物由于受本身的溶解性、辅料与工艺条件的影响,崩解后药物的溶出速率会影响疗效,
所以固体制剂需要进行溶出度检查。
检查方法:溶出度仪。
第一法为转篮法,第二法为桨法,第三法为小杯法。
(6)释放度:指口服药物从缓释制剂、控释制剂或肠溶制剂在规定溶剂中释放的速度和程度。
检查法:溶出度仪。第一法用于缓控释制剂,第二法用于肠溶制剂,第三法用于透皮贴剂。测定至少 3
个时间点的释放量。
(7)融变时限:融变时限是检查栓剂或阴道片等固体制剂在规定条件下的融化,软化或溶散的情况。
检查方法:融变时限仪。
(8)微生物限度:微生物限度检查法是检查非规定灭菌制剂及其原、辅料受微生物污染程度的方法,
检查项目包括细菌数、真菌数、酵母菌数及控制菌检查。
初级药师考试辅导 基础知识
第 14页
检查方法:微生物培养法。
(9)无菌检查法:无菌检查是检查药品、医疗器具、原料、辅料等无菌品种是否被微生物污染。
检查方法:薄膜过滤法、直接接种法。
(10)不溶性微粒:在澄明度检查符合规定后,用以检查静脉注射用溶液型注射液、静脉注射用无菌
粉末、静脉注射用浓溶液以及供静脉注射用无菌原料药中不溶性微粒的大小及数量。
检查意义:保证用药安全。
二、片剂、胶囊剂
片剂包括普通片、含片、舌下片、口腔贴片、咀嚼片、分散片、可溶片、泡腾片、阴道片、阴道泡腾
片、缓释片、控释片与肠溶片等。
检查项目:
● 多数片剂应进行重量差异和崩解时限检查;
● 口腔贴片应进行溶出度或释放度以及微生物检查;
● 咀嚼片不进行崩解时限检查;
● 分散片应进行溶出度和分散均匀性检查;
● 阴道片应进行融变时限和微生物检查;
● 阴道泡腾片作发泡量和微生物检查;
● 肠溶片检查释放度;
● 缓释片与控释片均应检查释放度;
胶囊剂分为硬胶囊、软胶囊、缓释胶囊、控释胶囊和肠溶胶囊。
● 除另有规定外,应进行装量差异和崩解时限检查;
● 缓、控释胶囊和肠溶胶囊应做释放度检查。
三、注射剂和滴眼剂
注射剂分为注射液、注射用无菌粉末与注射用浓溶液。
注射剂检查项目:
●除另有规定外,注射剂应进行装量、装量差异、渗透压摩尔浓度、可见异物、不溶性微粒、无菌、
热原或细菌内毒素检查。
滴眼剂检查项目:
●除另有规定外,眼用制剂应做可见异物、粒度、沉降体积比、装量、渗透压摩尔浓度和无菌检查。
(1)可见异物
是指存在于注射液、滴眼液中,在规定条件下目视可以观察到的不溶性物质,其粒径或长度通常大于
50μm
检查意义:注射液中若有不溶性微粒,使用后可能引起静脉炎、过敏反应,甚至堵塞毛细血管
检查方法:灯检法、光散射法
(2)热原或细菌内毒素检查
①热原反应:指输液过程中由于致热原进入人体后作用于体温调节中枢而引起的发热反应,体温可达
40℃以上,严重时可伴有恶心呕吐、头痛、四肢关节痛、皮肤灰白色、血压下降、休克甚至死亡。
主要致热原是细菌代谢物(内毒素),具有耐热性、不挥发性、水溶性、滤过性和吸附性的特点。因
此注射剂热原或细菌内毒素检查是保证注射剂安全性的重要质量指标,具有十分重要的临床意义。
检查方法:将一定剂量的供试品,静脉注入家兔体内,在规定时间内,观察家兔体温升高的情况,以
判定供试品中所含热原的限度是否符合规定。
②细菌内毒素:细菌内毒素主要来自革兰氏阴性细菌,主要成分为脂多糖,对人有致热反应,甚至导
致死亡。
检查方法:鲎试剂法
初级药师考试辅导 基础知识
第 15页
(3)渗透压
(4)溶液澄明度
(5)检漏
四、栓剂
检查项目:
●重量差异、融变时限和微生物限度
融变时限检查的意义:栓剂放入腔道后,在适宜的温度下应能融化、软化或溶散,才能产生局部或全
身作用,所以应作融变时限检查。
五、软膏剂、眼膏剂
软膏剂检查项目:
●粒度、装量、无菌和微生物限度
眼膏剂检查项目:
●粒度、金属性异物、重量差异、装量和无菌
六、气(粉)雾剂及喷雾剂
气雾剂应检查泄漏率、每瓶总揿次、每揿主药含量、雾滴(粒)分布、喷射速率、喷出总量、无菌、
微生物限度。
①泄漏率:泄漏率是体现阀门系统密封性的重要指标。泄漏率对每揿主药含量、含量均匀性、喷出药
物/液滴的粒径密切相关。
②每瓶总揿数:为保证每瓶气雾剂的给药次数不低于规定的次数,需要进行每瓶总揿数的测定。
③每揿主药含量:由于每揿主药含量是处方因素的综合体现,也是容器和阀门系统质量的体现。通过
对批间和批内每揿主药含量的测定,可以有效地控制产品的质量,保证临床给药的一致性,确保临床疗效。
④有效部位沉积率:由于气雾剂在使用中由于抛射剂的量不断减小、容器内的压力也随之降低,虽然
药物的含量均匀性可能符合要求,但正是由于压力的降低,使药物的有效部位沉积率与使用初期不一致,
所以气雾剂在质量控制中应该对单次给药条件下的有效部位沉积率以及装量规格进行检查。
七、颗粒剂
检查项目:
●粒度、干燥失重、溶化性、装量差异及装量等检查。
干燥失重检查的意义:
因水分的存在会严重影响颗粒剂的质量。故药典规定应测定颗粒剂的干燥失重。
溶化性检查的意义:
因颗粒剂的主要特点是溶出和吸收速度比较快,可直接吞服或冲入水中饮用。因此药典规定测定其溶
化性。
粒度检查的意义:
主药是以固体微粒形式存在的,分散粒径的大小影响制剂疗效的正常发挥,药物粒径越小,则药物更
容易发挥药效,因此,应进行粒度检查。
八、滴耳剂、滴鼻剂、洗剂、搽剂、凝胶剂
检查项目:
●装量、微生物限度检查。
●无菌检查:用于手术、耳部伤口、耳膜穿孔的滴耳剂、洗耳剂;用于手术或创伤的鼻用制剂;用于
烧伤、或严重创伤的凝胶剂。
初级药师考试辅导 基础知识
第 16页
九、透皮贴剂
透皮贴剂用于完整皮肤表面,药物从贮库中扩散出来,透过皮肤进入血液循环系统而发挥药效,其作
用时间由药物含量和渗透速率所决定。
检查项目:
●释放度
十、复方制剂分析
复方制剂:含有两种及两种以上的有效成分的药物制剂。
分析方法的研究设计:
①若各有效成分之间互不干扰,利用各成分的物理化学性质的差异,用专一性较强方法,可不经分离
直接分别测定各成分直接测定各成分。
②若各有效成分之间相互干扰,可经处理、分离后测定,或者采用 HPLC 法、计算分光光度法测定。选
择 1~2 个主成分测定以控制质量。
对于制剂的检查,下列说法中正确的是
A.口腔贴片进行崩解时限检查
B.注射剂一般检查包括装量差异检查
C.咀嚼片进行崩解时限检查
D.防腐剂的检查属于注射剂一般检查的范围
E.胶囊剂除另有规定外,进行重量差异检查
『正确答案』B
『答案解析』本题考点为片剂、注射剂及胶囊剂的一般检查项目。
注射剂的检查项目一般不包括
A.装量差异
B.澄明度
C.无菌
D.热原
E.防腐剂使用的量
『正确答案』E
『答案解析』此考点为注射剂的一般检查项目。
软膏剂的一般检查中不包括
A.粒度检查
B.装量检查
C.微生物限度
D.无菌检查
E.崩解时限
『正确答案』E
『答案解析』本题的考点是软膏剂的一般检查。用排除法解题。
片剂平均重量在 0.3g 或者 0.3g 以上的片剂的重量差异限度为
A.±7.5%
B.±5.0%
C.5.0%
初级药师考试辅导 基础知识
第 17页
D.±7.0%
E.±0.5%
『正确答案』B
『答案解析』中国药典规定片剂在 0.3g 或者 0.3g 以上的片剂的重量差异限度为±5.0%。
凡检查含量均匀度的制剂不再检查
A.崩解时限
B.重(装)量差异
C.溶出度
D.主药含量
E.释放度
『正确答案』B
『答案解析』此考点为药品检测方法要求。
药品检验工作的基本程序是
A.鉴别-检查-写出报告
B.鉴别-检查-含量测定-写出报告
C.检查-含量测定-写出报告
D.取样-检查-含量测定-写出报告
E.取样-鉴别-检查-含量测定-留样-写出报告
『正确答案』E
『答案解析』此答案为检验工作的基本程序。
药品中的杂质及其检查
考试要求:
细目 要点
1.药物中的杂质
(1)杂质的来源
(2)杂质的限量与限量检查
(3)一般杂质与特殊杂质的概念
2.检查的方法及原理 重金属、砷盐、氯化物、硫酸盐、铁盐、铵盐、干燥失重、水分、溶剂残留
重点:掌握杂质检查所用的反应试剂
一、药物中的杂质
1.杂质的来源:生产过程中引入、贮藏过程中引入。
2.杂质分类
一般杂质:指在自然界中分布较广泛,在多种药物的生产和贮藏过程中容易引入的杂质,如酸、碱、
水分、氯化物、硫酸盐、砷盐、重金属等。
特殊杂质:指在个别药物的生产和贮藏过程中引入的杂质,如阿司匹林在生产和贮存过程中会引入水
杨酸。
3.杂质限量与限量检查
杂质限量:指药物中允许杂质存在的最大量,通常用百分之几或百万分之几(ppm)来表示;
初级药师考试辅导 基础知识
第 18页
S:供试品的量,C:杂质标准溶液的浓度,V:杂质标准溶液的体积,L:杂质限量。
阿普唑仑中氯化物的检查
取本品 0.50g,加水 50ml,振摇 10 分钟,滤过,取续滤液 25ml,依法检查,与标准氯化钠溶液(10
μg Cl/ml)5.0ml 制成的对照液比较,不得更浓。求氯化物的限量。
检查溴化钠中的砷盐,规定含砷量不得过 0.0004%,取标准砷溶液 2.0ml(每 1ml 相当于 1μg 的 As)
制备标准砷斑,应取供试品
A.0.1g B.0.2g C.0.5g
D.1.0g E.2.0g
『正确答案』C
『答案解析』已知 L=0.0004%,V=2,C=1μg/ml,求 S;关键单位统一。
二、杂质检查方法与原理
1.重金属检查法
检查重金属:银、铅、汞、铜、镉、锡、锑、铋等能与硫代乙酰胺或硫化钠作用显色的金属。
《中国药典》重金属检查法一共收载有三法,以 Pb 为代表。
(1)硫代乙酰胺法
原理:
适用范围:适用于溶于水、稀酸和乙醇的药物
测定条件:
①每 1ml 含 10μgPb 的标准铅溶液,适宜比色范围为 10~20g/ml 的 Pb2+。
②用醋酸盐缓冲液(pH3.5)控制溶液 pH 值为 3~3.5。
③试剂:硫代乙酰胺。
(2)炽灼残渣法
适用范围:适用于含芳环、杂环以及难溶于水、稀酸及乙醇的有机药物。
原理:500~600℃炽灼后的残渣,经处理后,依第一法检查。
(3)硫化钠法
适用范围:溶于碱溶液,而不溶于酸溶液的药物。如磺胺类、巴比妥类。
原理:
重金属检查法的比较
硫代乙酰胺法 炽灼残渣法 硫化钠法
适用范 溶解后溶液澄清、无色的 难溶于水或能与重金属离子形成配位化合物 溶于碱而不溶于稀酸或在稀酸中
初级药师考试辅导 基础知识
第 19页
围 药物 的药物 生成沉淀的药物
原理
PbS 黄色—棕黑色
样品特
殊处理
无
炽灼→加硝酸→加盐酸→氨水调中性→硫代
乙酰胺反应
无
2.砷盐检查法
《中国药典》采用古蔡法和二乙基二硫代氨基甲酸银法检查药物中微量的砷盐。
古蔡法:
原理:是利用金属锌与酸作用产生新生态的氢,与药物中微量砷盐反应,生成具有挥发性的砷化氢气
体,遇溴化汞试纸,产生黄色至棕色的砷斑,与一定量标准砷溶液在相同条件下所生成的砷斑比较,来判
断药物中砷盐的含量。
二乙基二硫代氨基甲酸银法
原理:砷化氢与 Ag-DDC 吡啶溶液作用,使 Ag-DDC 中的银还原为红色胶态银,直接比色或于 510nm 波
长处测定吸收度,进行比较。
古蔡法 二乙基二硫代氨基甲酸银法
原理
第一步
第二步 砷化氢与溴化汞试纸反应→黄色至棕色斑点 砷化氢与二乙基二硫代氨基甲酸银反应→红色
标准溶液 标准砷溶液,1mgAs/ml,用量 1-2ml
反应试剂 溴化汞试纸 二乙基二硫代氨基甲酸银吡啶溶液
结果判断 目视比较色斑 510nm 测定吸光度
3、氯化物检查法
原理:利用氯化物在硝酸酸性溶液中与硝酸银试液作用,生成氯化银的白色混浊,比较。
测定条件:
1)标准 NaCl 溶液 10gCl-/ml,在测定条件下,以 50ml 中含 50~80μg 的 Cl-为宜,相当于标准 NaCl
溶液 5~8ml。——原因:在此范围内氯化物所显浑浊梯度明显,便于比较。
2)反应需在硝酸酸性条件下进行,且以 50ml 供试溶液中含稀硝酸 10ml 为宜。
加稀硝酸的目的:①避免弱酸银盐的沉淀的形成而干扰检查。
②加速氯化银沉淀的生成并产生较好的乳浊。
3)试剂:硝酸银。
初级药师考试辅导 基础知识
第 20页
4)供试液和对照液稀释后,再加硝酸银溶液,使生成白色浑浊而不是白色沉淀。
5)避光、暗处放置 5 分钟后比浊,——目的:防止 AgCl 见光分解。
6)比浊方法:同置于黑色背景上,自上向下观察。
4.硫酸盐检查法
原理:利用 SO4
2-与氯化钡在盐酸酸性溶液中生成硫酸钡的白色浑浊液,比较。
测定条件:
1)标准 K2SO4 溶液 0.1mg/ml,50ml 溶液中含 0.1~0.5mg 的所显浑浊梯度明显,相当于标准 K2SO4 溶液
1~5ml。
2)反应需在盐酸酸性条件下进行,且以 50ml 供试溶液中含稀盐酸 2ml 为宜。
加盐酸的目的:可防止碳酸钡或磷酸钡等沉淀的生成 。
pH 值约为 1 为宜——原因:若酸度过高,可使硫酸钡溶解度增大,检查的灵敏度下降。
3)试剂:氯化钡。
4)供试液和对照液稀释后,再加氯化钡溶液,使生成白色浑浊而不是白色沉淀。
5)比浊方法:同置于黑色背景上,自上向下观察。
5.铁盐检查法
原理:铁盐在盐酸酸性溶液中与硫氰酸铵生成红色可溶性硫氰酸铁配位离子,与对照比较。
测定条件:
1.用 FeNH4(SO4)2·12H2O(硫酸铁铵)配制标准铁贮备液(加入硫酸防止 Fe3+的水解),标准铁溶液
10g Fe3+/ml,50ml 溶液中含 10~50g 的 Fe3+显色梯度明显,一般取标准铁溶液 1.0~5.0ml。
2.反应需在盐酸酸性条件下进行,防止 Fe3+的水解.且以 50ml 供试溶液中含稀盐酸 4ml 为宜。
3.试剂:硫氰酸铵。加过量硫氰酸铵,使反应向正反应方向进行。
4.加氧化剂氧化 Fe2+为 Fe3+。加过硫酸铵可氧化 Fe2+为 Fe3+,同时可防止光线使硫氰酸铁还原或分解褪
色。
5.比色方法:同置于白色背景上,自上向下观察。
氯化物、硫酸盐、铁盐检查方法的比较
氯化物检查法 硫酸盐检查法 铁盐检查法
原理 白色
浑浊
白色
浑浊
Fe3+SCN-→Fe(SCN)6
红色
标准
溶液
NaCl 溶液,10mgCl-/ml,5-8ml K2SO4 溶液,0.1mg/ml,1-5ml
硫酸铁铵,10mg
Fe3+/ml,1-5ml
反应
试剂
硝酸银 氯化钡 硫氰酸铵(过量)
反应
条件
稀硝酸,10ml 稀盐酸,2ml
稀盐酸+氧化剂(过硫
酸铵),4ml
比色 黑色背景 黑色背景 白色背景
初级药师考试辅导 基础知识
第 21页
6.铵盐检查法
原理:将供试品中的铵盐碱化后蒸馏出来,与碱性碘化汞钾试液反应而呈色,与标准氯化铵溶液同法
显色进行比较。
7.干燥失重测定法
指药物在规定条件下经干燥后所减失的重量,主要是水分,也包括其他挥发性物质。
①常压恒温干燥法:一般 105℃
②干燥剂干燥法:硅胶、无水氯化钙和五氧化二磷
③减压干燥法:适用于熔点低,受热不稳定或水分难赶除的药物。
④热分析法:适用于结晶水的测定,也适用于贵重药物或在空气中易氧化药物干燥失重的测定。
8.费休氏水分测定法:水分系指用费休氏水分测定法测得药品中的残留水和结晶水的总和,不包括其
他挥发性物质。——仪器测定。
9.残留溶剂测定法
残留溶剂是指在原料药或辅料的生产中,以及在制剂制备过程中使用的,但在工艺过程中未能完全除
去的有机溶剂。
残留溶剂的检查方法
采用气相色谱法检查药物中的残留溶剂。
色谱柱:不同极性的毛细管柱或高分子多孔小球为填料的填充柱
载气:氮气
检测器:FID、ECD
供试品制备:顶空进样、溶液直接进样
色谱系统适用性试验:理论塔板数、分离度、重复性
测定方法:限度检查、定量测定
残留溶剂的分类
第一类溶剂是应该避免使用的溶剂,一般为致癌物或危害环境的物质。如苯、四氯化碳。
第二类溶剂是应限量使用的溶剂,一般具有非基因毒性,不可逆或可逆毒性。如甲苯、甲醇、正己烷、
乙腈。
第三类溶剂是毒性低,对人体危害较小,推荐使用的溶剂。
第四类溶剂是目前尚无足够毒理学资料的溶剂。如石油醚、异丙醚等。
试题分析
重金属杂质的代表是
A.铅
B.铜
C.银
D.锌
E.汞
『正确答案』A
试题分析
重金属检查法中,所使用的醋酸盐缓冲液的 pH 值是
A.1.5
B.2.5
C.3.5
D.4.5
初级药师考试辅导 基础知识
第 22页
E.5.5
『正确答案』C
试题分析
以下有机溶剂中,属于第一类溶剂的有
A.苯
B.甲苯
C.二氯甲烷
D.三氯甲烷
E.四氯甲烷
『正确答案』AE
可用于检查的杂质为
A.氯化物 B.砷盐
C.铁盐 D.硫酸盐 E.重金属
1.在酸性溶液中与氯化钡生成浑浊液的方法
『正确答案』D
2.在酸性溶液中与硫氰酸盐生成红色的方法
『正确答案』C
3.在实验条件下与硫代乙酰胺形成均匀混悬溶液的方法
『正确答案』E
可用于检查的杂质为
A.氯化物 B.砷盐
C.铁盐 D.硫酸盐 E.重金属
4.Ag-DDC 法
『正确答案』B
5.古蔡法
『正确答案』B
『答案解析』此题考察的是各种杂质检查的方法。题 1 检查的是硫酸盐,利用硫酸根与氯化钡反应。
题 2 选 C。利用三价铁与硫氰酸铵生成红色配合物。题 3 检查的是重金属,属于重金属检查的第一法。
题 4 检查的是砷盐,属于砷盐检查的第二法。题 5 检查的也是砷盐,属于砷盐检查的第一法。
药品分析方法的要求
细目 要点
1.准确度
(1)含量测定方法的准确度
(2)杂质定量测定的准确度
(3)数据要求
2.精密度
(1)重复性
(2)中间精密度
(3)重现性
(4)数据要求
3.专属性 (1)鉴别反应
初级药师考试辅导 基础知识
第 23页
(2)含量测定及杂质检查
4.检测限
(1)信噪比法
(2)数据要求
5.定量限 概念
6.线性
(1)概念
(2)数据要求
7.范围
(1)概念
(2)有关规定
8.耐用性 概念
重点:准确度、精密度、定量限
一、准确度
准确度是指用该方法的测定结果与真实值或参考值接近的程度。准确度一般用回收率(%)来表示。
1.方法:将已知量的测定组分加入到处方比例的附加剂中,用验证的方法进行测定,根据测定结果计
算回收率。
2.杂质定量测定中的准确度:采用原料药或制剂中加入已知量杂质进行测定;如不能得到杂质或降解
产物,可与另一成熟方法进行比较,如药典方法或经过验证的方法。
3.含量测定中的准确度:测定原料药时,可用已知纯度的对照品或样品进行测定,或用本法所得结果
与建立准确度的另一方法测定的结果进行比较。
4.数据要求:测定高、中、低三个浓度,n=3,共 9 个数据来评价回收率的 RSD<2%;用 UV 和 HPLC 法
时,一般回收率可达 98%~102%;容量法可达 99.7%~100.3%。
二、精密度
1.精密度是指在规定的测试条件下,同一个均匀样品,经多次取样测定所得结果之间的接近程度。精
密度一般用偏差、标准偏差(SD)或相对标准偏差(RSD)来表示。偏差、标准偏差(SD)或相对标准偏差
(RSD)越小,精密度越好。
2.精密度与准确度的关系:精密度好是准确度高的前提,但方法的精密度好,准确度不一定高。
要求:定量测定应考察方法的精密度。
3.考查内容包括:
重复性:在相同条件下,由一个分析人员测定所得结果的精密度。
中间精密度:在同一个实验室,不同时间由不同分析人员用不同设备测定结果的精密度。
重现性:在不同实验室由不同分析人员测定结果的精密度。
三、专属性
1.指在其他组分(如杂质、降解产物、辅料等)可能存在的情况下,分析方法能准确地测出被测组分
的特性。
2.鉴别反应的专属性:应能与其他共存的物质或相似化合物区分,不含被测组分的样品均应呈现负反
应。
3.含量测定和杂质检查的专属性:
含量测定的专属性:附代表性的图谱,以说明专属性,图中应注明各组分的位置,色谱法中分离度应
符合要求。
初级药师考试辅导 基础知识
第 24页
杂质鉴定的专属性:
①杂质可获得:可向供试品中加入一定量的杂质;
②杂质或降解产物不能获得:通过与另一种已证明合理但分离或检测原理不同或具较强分辨能力的方
法进行结果比较来确定,或比较破坏前后检出的杂质个数和量。
四、检测限
指分析方法在规定的实验条件下所能检出被测组分的最低浓度或最低量。
目视法:非仪器法
信噪比法:2 倍噪音或 3 倍噪音对应的样品浓度或量。
五、定量限
指样品中被测组分能被定量测定的最低浓度或最低量。
10 倍噪音对应的浓度或量。
六、线性
在设计范围内,测试结果和样品中被测组分的浓度(或量)直接成正比关系的程度。
考察的方法:配制一系列不同浓度的测定组分溶液(至少 5 份),分别测定其响应值,用最小二乘法
以响应值对浓度进行线性回归,即可计算出相关系数 r 和 a、b 的值。
七、范围
指在达到一定的精密度、准确度和线性的前提下,分析方法适用的高、低浓度或量的区间。
相关规定:含量测定的范围应为测试浓度的 80%~100%或更宽;
制剂含量均匀度检查,范围应为测试浓度的 70%~130%;
溶出度或释放度中的溶出量,范围应为限度的±20%;
杂质测定时,范围应根据初步实测结果,拟订出规定限度±20%。
八、耐用性
指在测定条件有小的变动时,测定结果不受其影响的承受程度。
不同的检验项目对方法验证指标的要求有所不同
初级药师考试辅导 基础知识
第 25页
效能指标 鉴别
杂质检查
含量测定
定量测定 限量检查
准确度 - + - +
精密度 - + - +
专属性 + + + +
检测限 + - + -
定量限 - + - -
线性 - + - +
范围 - + - +
耐用性 + + + +
在规定的测试条件下、同一个均匀样品经多次取样测定,所得结果之间的接近程度称为
A.准确度
B.精密度
C.专属性
D.检测限
E.线性
『正确答案』B
【B 型题】A.分析方法的测定结果与真实值或参考值接近的程度
B.同一均匀样品经多次取样测定所得结果之间的接近程度
C.在其他组分可能存在的情况下,分析方法能准确地测出被测组分的能力
D.分析方法所能检出试样中被测组分的最低浓度或最低量
E.分析方法可定量测定试样中被测组分的最低浓度或最低量
分析方法验证指标的定义是
1.精密度
2.检测限
『正确答案』B、D
『答案解析』考察药品质量标准分析方法验证内容的概念。A 为准确度,C 为专属性,E 为定量限。
确定分析方法的检测限时,一般要求信噪比为
A.1:1
B.3:1
C.5:1
D.10:1
E.20:1
『正确答案』B
典型药物的分析
细目 要点
1.苯巴比妥
(1)鉴别:丙二酰脲反应
(2)有关物质检查
初级药师考试辅导 基础知识
第 26页
(3)含量测定:银量法
2.阿司匹林
(1)鉴别:三氯化铁反应
(2)游离水杨酸的检查
(3)含量测定:酸碱滴定法
3. 普鲁卡因
(1)鉴别:重氮化-偶合反应
(2)对氨基苯甲酸的检查
(3)含量测定:亚硝酸钠滴定法
4.异烟肼
(1)鉴别:与硝酸银的反应
(2)游离肼的检查
(3)含量测定:HPLC 法
5.地西泮
(1)鉴别:与浓酸的呈色反应、氯化物的鉴别反应
(2)有关物质检查
(3)含量测定:非水溶液滴定法
6. 硫酸阿托品
(1)鉴别:托烷生物碱的反应
(2)有关物质的检查
(3)含量测定:非水溶液滴定法
7.维生素 C
(1)鉴别:与硝酸银的反应
(2)金属杂质的检查
(3)含量测定:碘量法
8.阿莫西林
(1)鉴别:HPLC 法
(2)聚合物的检查
(3)含量测定:HPLC 法
9.氢化可的松
(1)鉴别:与硫酸的呈色反应
(2)含量测定:HPLC 法
(3)杂质检查
10.地高辛
(1)鉴别:Keller-Kiliani 反应
(2)有关物质检查
(3)含量测定:HPLC 法
重点:有特点的鉴别方法(反应试剂)
特殊的含量测定方法
一、苯巴比妥的分析
结构特点及鉴别特征:
1.环状丙二酰脲结构——碱性条件下,与重金属离子反应
2.苯环——苯环特征反应
(一)鉴别反应
1.与重金属离子的反应——丙二酰脲的特征反应
与银盐的反应:取供试品约 0.1g,加碳酸钠试液 1ml 与水 10ml,振摇 2min,滤过,滤液中逐滴加入硝
酸银试液,即白色沉淀,振摇,沉淀即溶解;继续滴加过量的硝酸银试液,沉淀不再溶解。
(一银盐溶于水,二银盐不溶)
与铜盐的反应:取供试品约 50mg,加吡啶溶液
(1→10)5ml,溶解后,加铜吡啶试液(硫酸铜 4g,水 90ml 溶解后,加吡啶 30ml,即得)1ml,即显
紫色或生成紫色沉淀。
初级药师考试辅导 基础知识
第 27页
(二)有关物质检查
检查项目:干燥失重、炽灼残渣、酸度、乙醇溶液的澄清度、中性或碱性物质、有关物质。
(三)含量测定
银量法:反应原理同“银盐的反应”。
用硝酸银滴定液(0.1mol/L)滴定,以电位法指示终点。
二、阿司匹林的分析
(一)鉴别反应
三氯化铁反应:阿司匹林分子中具有酯结构,加水煮沸水解后生成水杨酸,水杨酸可与三氯化铁反应
生成紫堇色的配位化合物。
(二)杂质检查
游离水杨酸检查——HPLC 法。
(三)含量测定
《中国药典》采用酸碱滴定法测定阿司匹林含量。
溶剂:中性乙醇
滴定液:氢氧化钠滴定液
指示剂:酚酞
反应摩尔比:1:1——滴定度 18.02(mg/ml)
三、普鲁卡因的分析
1.鉴别反应
芳香第一胺反应
又称重氮化-偶合反应,用于鉴别芳香第一胺
(即芳伯氨)
芳伯氨基,在盐酸介质中与亚硝酸钠作用,生成重氮盐,重氮化盐进一步与β-萘酚偶合。生成有色偶
氮合物沉淀(由粉红色到猩红色)。
2.检查
特殊杂质:对氨基苯甲酸——HPLC 法。
3.含量测定
盐酸普鲁卡因分子结构中含有芳香伯胺,《中国药典》采用亚硝酸钠滴定法进行含量测定,用永停法
指示终点。
溶剂:盐酸,加溴化钾
滴定液:亚硝酸钠滴定液
终点判断:永停法
反应摩尔比:1:1
初级药师考试辅导 基础知识
第 28页
四、异烟肼的分析
(一)鉴别
与氨制硝酸银试液的反应——酰肼基的还原性;
异烟肼的酰肼基具有还原性,与硝酸银反应,生成气泡与黑色浑浊,并在试管壁上生成银镜。
(二)检查
游离肼的检查
薄层色谱法,对二甲氨基苯甲醛试液显色。要求在供试品主斑点前方与对照品溶液主斑点相应的位置
上,不得显黄色斑点。控制限量为 0.02%。
(三)含量测定
高效液相色谱法。
五、地西泮的分析
(一)鉴别
(1)与硫酸的反应
地西泮加硫酸溶解后,在紫外光灯(365nm)下检视,显黄绿色荧光。
(2)氯化物检查
(二)有关物质的检查
有关物质
(三)含量测定
地西泮二氮杂环上的氮原子有弱碱性,采用非水溶液滴定法测定。
溶剂:冰醋酸-醋酐
滴定液:高氯酸滴定液
指示剂:结晶紫指示剂
初级药师考试辅导 基础知识
第 29页
六、硫酸阿托品的分析
(一)鉴别
1.托烷生物碱的反应(Vitali 反应)——托烷类生物碱的专属鉴别反应。
醇制 KOH
反应机理:硫酸阿托品→水解为莨菪酸+发烟硝酸→黄色的三硝基衍生物+醇制氢氧化钾→深紫色醌型
产物。
(二)有关物质的检查
茛菪碱:旋光度法。
阿托品为外消旋体,莨菪碱为左旋体。
(三)含量测定
阿托品具有碱性,《中国药典》采用非水溶液滴定法测定其含量。
溶剂:冰醋酸-醋酸酐
滴定液:高氯酸滴定液
指示剂:结晶紫指示液
特别注意:由于硫酸的酸性强,因此生物碱的硫酸盐在冰醋酸的介质中只能被滴定至生物碱的硫酸氢
盐。反应的摩尔比为 1:1。
七、维生素 C 的分析
(一)鉴别
与硝酸银试液的反应
初级药师考试辅导 基础知识
第 30页
维生素 C 分子中的二烯醇基具有较强的还原性,可被 Ag+氧化为去氢抗坏血酸,同时产生黑色的单质银
沉淀。
(二)金属杂质的检查
铁和铜
原子吸收分光光度法
248.3nm 是铁的分析线波长。采用标准加入法检查,限量为百万分之二。
324.8nm 是铜的分析线波长。采用标准加入法检查,限量为百万分之五。
(三)含量测定
维生素 C 具有还原性,《中国药典》采用碘量法测定维生素 C 的含量。
溶剂:新沸过的冷水+稀醋酸
原因:加入稀醋酸可使滴定时维生素 C 受空气中氧的氧化作用减慢,使用新沸过的冷水作为溶剂,是
为了减少水中溶解的氧对测定的影响。
滴定液:碘滴定液
指示剂:淀粉指示液
反应摩尔比:维生素 C∶碘滴定液= 1∶1
测定维生素 C 注射液时,先要加入丙酮,以消除注射液中含有的抗氧剂亚硫酸氢钠对测定的影响。
八、阿莫西林的分析
(一)鉴别
红外光谱法
(二)聚合物的检查
阿莫西林聚合物:分子排阻色谱法,葡聚糖凝胶 G-10(40~120μm)为填充剂,测定波长为 254nm。
(三)含量测定
高效液相色谱法,用十八烷基硅烷键合硅胶为填充剂,阿莫西林对照品,外标法定量。
九、氢化可的松的分析
(一)鉴别反应
与强酸的呈色反应:氢化可的松能与硫酸发生呈色反应,并形成绿色荧光。
(二)含量测定 HPLC 法
(三)杂质检查 HPLC 法检查“其他甾体”。
对于一个甾体激素药物,含量测定和杂质检查一般是在同一色谱条件下进行。
十、地高辛的分析
(一)鉴别
K-K 反应:α-去甲基糖类的反应。将甾体强心苷溶于含有微量 FeCl3(1 滴 9%的 FeCl3)的冰醋酸 1-2ml
中,沿管壁缓缓加入浓硫酸 1-2ml,使成两液层。两液层接界面显棕色;醋酸层显蓝色或蓝绿色,放置 1 小
时后显靛蓝色。
(二)检查
有关物质检查:HPLC 法
(三)含量测定
HPLC 法
【A 型题】具芳伯氨基的芳胺类药物,重氮化反应的适宜条件是
A.弱碱性
B.中性
初级药师考试辅导 基础知识
第 31页
C.碱性
D.酸性
E.强酸性
『正确答案』D
『答案解析』考查重氮化反应,其实质是考察亚硝酸钠滴定法的反应条件。反应需要在酸性介质中进
行。加入过量的盐酸可加快反应的速度,使重氮盐在酸性溶液中稳定,同时可防止重氮氨基化合物的
形成。但酸度也不宜过高,否则阻碍芳伯氨基的游离,反而影响重氮化反应速度。
【A 型题】供试品与硝酸共热得黄色产物,放冷后加醇制氢氧化钾少许即显深紫色。此反应可鉴别的药
物是
A.盐酸麻黄碱
B.硫酸阿托品
C.盐酸吗啡
D.硫酸奎宁
E.硝酸士的宁
『正确答案』B
『答案解析』考查硫酸阿托品的鉴别方法。解此题的关键是把握题目中的关键试剂——硝酸、醇制氢
氧化钾。这是托烷类生物碱的专属特征反应,选项中阿托品为托烷类生物碱。所以答案选 B。
使用碘量法测定维生素 C 的含量,已知维生素 C 的分子量为 176.13,每 1ml 碘滴定液(0.1mol/L),
相当于维生素 C 的量为
A.17.61mg
B.8.806mg
C.176.1mg
D.88.06mg
E.1.761mg
『正确答案』A
『答案解析』考查维生素 C 的含量测定方法。维生素 C 由于具有还原性,可以用碘量法进行测定。反
应中 1mol 的维生素需要消耗 1mol 的碘滴定液。1ml 碘滴定液(0.1mol/L)为 0.1mol,可以和 0.1mol
的维生素 C 反应,所以对应的维生素 C 的质量为 0.1mol*176.13=17.61mg,答案为 A。
体内药物分析法
考试要求:
细目 要点
1.生物样品前处理方法
(1)蛋白质的去除
(2)组织的酶解法
(3)样品的分离与纯化
(4)浓集
2.常用的检查方法
(1)对检测方法的要求
(2)常用检测方法及特点
3.生物样品测定方法的基本要求
(1)专属性
(2)标准曲线和线性范围
(3)精密度和准确度
初级药师考试辅导 基础知识
第 32页
(4)定量下限
(5)样品稳定性
(6)提取回收率
(7)质控样品
(8)质量控制
4.体内药物分析在医院中的应用
药物的体内过程:
体内样品的种类
体内分析的特点:
①样品复杂,干扰物质多
②样品量少,药物浓度低
③工作量大,测定数据的处理和阐明不太容易
一、生物样品的前处理
(一)蛋白质的去除
1.去除蛋白质的意义:
①释放结合型药物,以便测定药物的总浓度;
②预防提取过程中蛋白质发泡,减少乳化的形成;
③保护仪器性能,延长使用期限。
2.去除蛋白质的方法:
蛋白质沉淀法
加与水混溶的有机溶剂脱水
加入强酸生成不溶性盐
加无机盐盐析
(二)组织的酶解法
在测定一些酸不稳定及与蛋白质结合牢的药物时,常需要酶解法。最常用的酶是蛋白水解酶中的枯草
菌溶素,它可使组织酶解,使药物析出。
(三)样品的分离与纯化
分离、纯化、浓缩的意义——提高分析的特异性和灵敏度。
初级药师考试辅导 基础知识
第 33页
常用方法:
液-液萃取——选用与水不相混溶的有机溶剂进行提取
有机溶剂的种类
pH 值的选择
固相萃取法——利用柱色谱进行分离
固相萃取法:
利用吸附剂将生物样品中的药物吸附,与样品的基质和干扰化合物分离,然后再用洗脱液洗脱,达到
分离或者富集目标化合物的目的。
选择固相萃取小柱
活化——加样——洗涤——洗脱
(四)浓集的方法:
减少萃取液用量
挥去溶剂
二、常用的检测方法
1.对检测方法的要求:高灵敏度、高专属性。
2.常用方法:
灵敏度 专属性 适用范围
免疫分析法 ++++ ++ 临床药物监测
色谱分析法 +++ +++ 药代动力学
初级药师考试辅导 基础知识
第 34页
三、生物样品测定方法的基本要求
1.专属性
分析方法测量和区分共存组分中分析物的能力,即能证明所测的药为原型物或其代谢物,并能排除某
些内源性物质和杂质的干扰。
要求:
色谱法至少要考察 6 个不同个体空白生物样品色谱图、空白生物样品外加对照物质色谱图(注明浓度)
及用药后的生物样品色谱图。
以软电离质谱为基础的检测方法(LC-MS、LC-MS/MS 等),考察分析过程中的基质效应,如离子抑制
等。
2.标准曲线与线性范围
分析物浓度与试验响应值间的相关性,在线性范围内浓度测定结果应达到试验要求的精密度和准确度。
要求:用至少 6 个浓度建立标准曲线,应使用与待测样品相同的生物介质,线性范围要能覆盖全部待
测浓度,不允许将定量范围外推求算未知样品的浓度。标准曲线时不包括零点。
3.精密度与准确度
精密度:在确定的分析条件下,相同介质中相同浓度样品的一系列测量值的分散程度。
准确度:在确定的分析条件下,测得值与真实值的接近程度。
方法:选择 3 个浓度的质控样品同时进行方法的精密度和准确度考察。低浓度选择在定量下限附近,
高浓度接近于标准曲线的上限附近;中间选一个浓度。每一浓度每批至少测定 5 个样品。
精密度用质控样品的批内和批间相对标准差(RSD)表示,相对标准差一般应小于 15%,在定量下限附
近相对标准差应小于 20%。
初级药师考试辅导 基础知识
第 35页
准确度用相对回收率表示,即采用“回收试验”或“加样回收试验”得到药物在样品中的回收率,一
般应在 85%~115%范围内,在最低定量限附近应在 80%~120%范围内。
4.定量下限
标准曲线上的最低浓度点,也称灵敏度;
要求:至少能满足测定 3~5 个半衰期时样品中的药物浓度,或 Cmax 的 1/10~1/20 时的药物浓度,其准
确度应在真实浓度的 80%~120%范围内,RSD 应小于 20%。应由至少 5 个标准样品测试结果证明。
5.样品稳定性
表示一种分析物在确定条件下,一定时间内在给定介质中的化学稳定性。
要求:根据具体情况,对含药生物样品在室温、冰冻或冻融条件下以及不同存放时间进行稳定性考察,
以确定生物样品的存放条件和时间。还应注意储备液的稳定性以及样品处理后的溶液中分析物的稳定性。
6.提取回收率:分析过程的提取效率,能反映出样品预处理过程中组分丢失的情况,是评价萃取方案
优劣的指标之一,以样品提取和处理过程前后分析物含量百分比表示。应考察高、中、低 3 个浓度的提取
回收率,其值一般低于 100%(可能低至 60%),但重要的是重现性要好。
7.质控样品:系指在生物介质中加入已知量待测药物所配制的样品,用于质量控制。
8.质量控制:在生物样品分析方法确证完成之后开始测试未知样品,每个未知样品一般测定一次,必
要时可进行复测。每批生物样品测定时应建立新的标准曲线,并随行测定高、中、低 3 个浓度的质控样品,
每个浓度多重样本。质控样品测定结果的偏差一般应小于 15%,最低浓度点偏差应小于 20%。
四、体内药物分析在医院中的应用
药物监测——治疗药物、易中毒的药物
临床毒物分析
疾病诊断
药代动力学与生物药剂学研究
试题分析
临床治疗药物监测中最常用的样本是
A.脏器
B.组织
C.血浆
D.汗液
E.尿液
『正确答案』C
相关文档
- 3篇主任医师述职报告供借鉴2021-05-27 23:08:088页
- 妇产科医师年度工作总结五篇范文2021-05-27 22:51:308页
- 精编国家开放大学电大专科《医学免2021-05-27 22:30:156页
- 医学院XX年春季学期工作总结2021-05-27 22:17:545页
- 住院医师规培年度总结范文2021-05-27 21:49:024页
- 药师工作自我鉴定【三篇】2021-05-27 21:40:062页
- 精编国家开放大学电大专科《医学免2021-05-27 20:55:254页
- 主治医师年度述职报告_医院述职2021-05-27 20:11:067页
- 2019医师年度考核个人总结范文2021-05-27 19:55:053页
- 医学生实习心得体会精编范文【四篇2021-05-27 18:49:196页