- 108.00 KB
- 2021-04-15 发布
- 1、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 2、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报QQ:3215808601
气体摩尔体积
【学习目标】
1、理解气体摩尔体积的含义。
2、掌握气体摩尔体积的有关计算。
【要点梳理】
要点一、 影响物质体积大小的因素
1.影响物质体积大小的因素:
从微观来看,影响物质体积大小的因素有三个:微粒个数、微粒大小、微粒间距离。
1 mol任何物质中的粒子数目都是相同的,即约为6.02×1023。因此,1 mol物质的体积大小主要取决于构成物质的粒子的大小和粒子之间的距离。
2. 影响固体(或液体)物质体积大小的主要因素有两个:微粒个数和微粒自身大小
要点诠释:
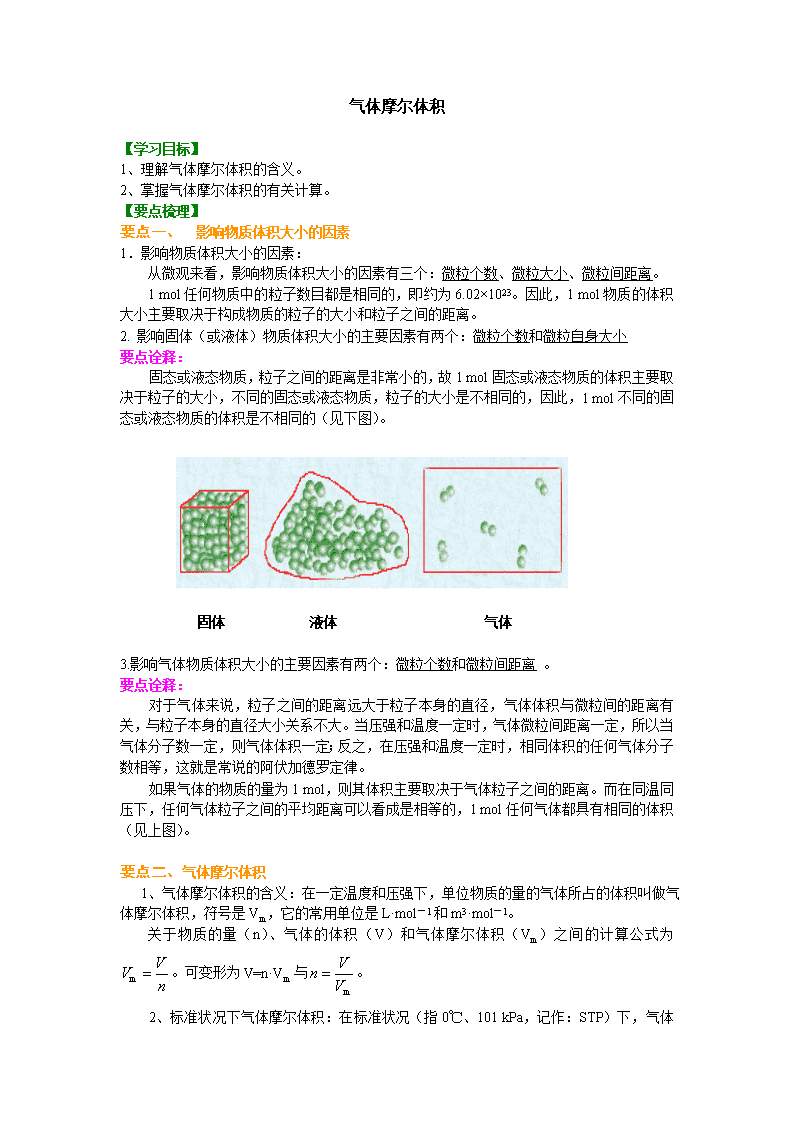
固态或液态物质,粒子之间的距离是非常小的,故1 mol固态或液态物质的体积主要取决于粒子的大小,不同的固态或液态物质,粒子的大小是不相同的,因此,1 mol不同的固态或液态物质的体积是不相同的(见下图)。
固体 液体 气体
3.影响气体物质体积大小的主要因素有两个:微粒个数和微粒间距离 。
要点诠释:
对于气体来说,粒子之间的距离远大于粒子本身的直径,气体体积与微粒间的距离有关,与粒子本身的直径大小关系不大。当压强和温度一定时,气体微粒间距离一定,所以当气体分子数一定,则气体体积一定;反之,在压强和温度一定时,相同体积的任何气体分子数相等,这就是常说的阿伏加德罗定律。
如果气体的物质的量为1 mol,则其体积主要取决于气体粒子之间的距离。而在同温同压下,任何气体粒子之间的平均距离可以看成是相等的,1 mol任何气体都具有相同的体积(见上图)。
要点二、气体摩尔体积
1、气体摩尔体积的含义:在一定温度和压强下,单位物质的量的气体所占的体积叫做气体摩尔体积,符号是Vm,它的常用单位是L·mol-1和m3·mol-1。
关于物质的量(n)、气体的体积(V)和气体摩尔体积(Vm)之间的计算公式为。可变形为V=n·Vm与。
2、标准状况下气体摩尔体积:在标准状况(指0℃、101
kPa,记作:STP)下,气体摩尔体积约为22.4 L·mol-1。
要点诠释:
①气体摩尔体积和标准状况下气体摩尔体积是两个不同的概念。前者是指单位物质的量气体所占的体积。后者是指标准状况下,1 mol气体所占的体积,这个体积数值约为22.4 L。所以用到22.4 L·mol-1时,通常是标准状况下的气体。
②气体摩尔体积中的气体指任意气体,该气体可以是纯净物,也可以是混合物;纯净物中,可以是单质,也可以是化合物。如标准状况下。1 mol氢气和氯气的混合气体的体积约为22.4 L,所含的分子总数为NA个。
③在掌握气体摩尔体积时要注意4个要点:(1)标准状况;(2)1mol;(3)任何气体,(包括单一气体或混合气体);(4)约22.4L。
3、气体体积(V)、气体摩尔体积(Vm)、气体的物质的量(n)之间关系为:
由n=N/NA和n=V/Vm,可将气体分子数与宏观气体体积之间联系起来。如标准状况下,11.2 L H2所含分子数为:
。
由一定条件下的密度和气体摩尔体积可以求出气体的摩尔质量:M=Vm·ρ 如标准状况下,ρ(O2)=1.429 g·L―1,则M (O2)=Vm·ρ(O2)=22.4 L·mol―1×1.429 g·L―1=32 g·mol―1。
4、标准状况下的相关计算。
M与Vm的关系:M=Vm·=22.4 g/mol;
n与Vm的关系:;
m与Vm的关系:;
N与Vm的关系:。
要点三、阿伏加德罗定律及其推论
1、定律内容:在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子数。这一规律称为阿伏加德罗定律。
要点诠释:
(1)阿伏加德罗定律只适用气体,对固体、液体物质不适用。
(2)只有温度、压强、体积都相同的气体,其分子数才相同。
(3)气体摩尔体积是阿伏加德罗定律的特殊情况和具体体现。
2.几个重要的推论:
(1)同温同压下,同体积的任何气体的质量比等于它们的相对分子质量之比。
(2)同温同压下,任何气体的体积比等于它们的物质的量之比。
(3)同温同压下,相同质量的任何气体的体积比等于它们的相对分子质量的反比。
(4)同温同压下,任何气体的密度比等于它们的相对分子质量之比。
(5)同温同容下,气体的压强比等于它们的物质的量之比。
规律总结:
①凡涉及物质的体积,要首先分辨出该物质是不是气体,看清条件是否为标准状况。
②同温同压下,相同体积的气体所含的分子数相同,但原子数不一定相同。
【典型例题】
类型一、气体摩尔体积
例1.下列说法正确的是( )
A.32 g O2占有的体积约为22.4 L
B.22.4 L N2含有阿伏加德罗常数个氮分子
C.在标准状况下,22.4 L水的质量约为18 g
D.22 g二氧化碳与标准状况下11.2 L HCl含有相同的分子数
【思路点拨】22.4L的使用有特定的范围:①物质必须为气体;②在标准状况下。
【答案】D
【解析】A、B两项都没有“标准状况”是错误的;C项虽有“标准状况”,但在此条件下水是液体,所以22.4 L水不是1 mol,故也不是18 g;D项中22 g CO2的物质的量为0.5 mol;标准状况下11.2 L HCI的物质的量也为0.5 mol,两种气体的物质的量相同,所以含有的分子数也相同,因此选项D符合题意。
【总结升华】只要用到体积,就要考虑温度、压强;只要用到“22.4 L·mol-1”,就要弄清是否是标准状况、是否是气体。审题一定要准。
举一反三:
【变式1】 下列说法中正确的是( )
A、标准状况下,98克硫酸的体积约为22.4升
B、1molO2的体积约为22.4升
C、22克CO2在标准状况下的体积为11.2升
D、分子数相同O2与SO2所占的体积相同
【答案】C
【变式2】下列说法中不正确的是( )
A.HCl的相对分子质量与6.02×1023个HCl分子的质量(以g为单位)在数值上相等
B.6.02×1023个氮分子和6.02×1023个氢分子的质量比等于14∶1
C.32 g氧气所含的原子数目为2×6.02×1023
D.常温常压下,0.5×6.02×1023个一氧化碳分子所占体积是11.2 L
【答案】D
【解析】摩尔质量在数值上等于该物质的相对原子质量或相对分子质量,也等于该物质所含6.02×1023个粒子的质量,A正确;相同数目的两种分子的质量比应等于其相对分子质量比,B正确;O2是双原子分子,32 g O2所含原子数是分子数的2倍,C正确;0.5×6.02×1023个CO分子即0.5 mol,所占体积在标准状况时才是11.2 L,D选项不正确。
【变式3】下列叙述正确的是
A.1 mol 任何气体的体积都约为22.4 L
B.1 mol 任何物质在标准状况下所占的体积都约是22.4 L
C.标准状况下,1 mol 水所占有的体积是22.4 L
D.标准状况下,22.4 L的任何气体的物质的量都约是1 mol
【答案】D
【变式4】下列叙述中,正确的是( )
A.在标准状况下,1molH2O的体积约为22.4L
B.在标准状况下,0.5molH2、0.5molN2组成的混合气体的体积约为22.4L
C.在非标准状况下,1mol任何气体的体积不可能为22.4L
D.标准状况下,气体的摩尔体积为22.4L
【答案】B
类型二、阿伏加德罗定律及其推论
例2.下列两种气体的分子数一定相等的是( )
A.质量相等、密度不等的N2和CO
B.等体积、等密度的CO和NO
C.等温、等体积的O2和N2
D.等压、等体积的N2和CO2
【思路点拨】依据阿伏加德罗定律可知,相同条件(温度、压强)下,气体的体积相等则分子数(或物质的量)一定相等。
【答案】A
【解析】B中,由m=V可知二者质量相等,但M (CO)≠M (NO),故二者物质的量n (CO)≠n (NO),其分子数不相等;C中,压强不确定,则分子数不确定;D中,温度不确定,分子数也无法确定;而A中,由于二者摩尔质量相等,质量相等,则n (N2)=n (CO)。
【总结升华】只要用到体积,就要考虑温度、压强。
举一反三:
【变式1】标准状况下两个容积相等的贮气瓶,一个装有02,另一个装有CH4,两瓶气体具有相同的( )
A.质量 B.原子总数 C.密度 D.分子数
【答案】D
【变式2】两个体积相同的容器,一个盛有NO,另一个盛有N2和O2,在同温同压下两容器内的气体一定具有相同的
A.原子总数 B.质子总数 C.分子总数 D.质量
【答案】AC
【变式3】下列条件下,两种气体的分子数一定不相等的是( )
A.相同质量、不同密度的N2和C2H4
B.相同体积、相同密度的CO和C2H4
C.相同温度、相同压强、相同体积的O2和N2
D.相同压强、相同体积、相同质量的O2和N2
【答案】D
【解析】A项N2和C2H4的摩尔质量相同,相同质量的N2和C2H4,物质的量相同,分子数也相同;B项相同体积、相同密度的CO和C2H4,具有相同的质量,同时也具有相同的分子数;C项同温同压下同体积的任何气体具有相同的分子数;D项同质量的O2和N2,摩尔质量不同,物质的量不同,从而分子数不相等,故选D。
【高清课堂:气体摩尔体积练一练2】
【变式4】在同温、同压、相同质量的下列气体占有的体积由大到小的顺序是:
①Cl2 ②N2 ③ H2 ④ CO2 ⑤ O2
【答案】③>②>⑤>④>①
【解析】由阿伏伽德罗定律,在同温、同压下气体的体积与物质的量成正比,质量相同时物质的量与摩尔质量成反比。
【变式5】150 mL A2气体跟50 mL B2气体恰好完全反应,生成的气体体积为100 mL(同温、同压条件下),试填空:
(1)生成物的化学式是________。
(2)推断化学式的依据是________。
【答案】(1)A3B (2)阿伏加德罗定律和质量守恒定律
【解析】设生成物的化学式为AxBy,依题意反应物与生成物的体积比:V(A2)∶V(B2)∶V(AxBy)=150∶50∶100=3∶1∶2。根据阿伏加德罗定律,可知这个3∶1∶2既是体积比,又是物质的量之比,也是化学方程式的化学计量数之比,即可写出化学方程式的表示式:3A2+B2===2AxBy,又根据质量守恒定律可知反应前后各元素的原子个数不变,即在反应物中A的原子数是2×3,B的原子数是2,所以2AxBy应为2A3B。
类型三、计算
例3、在标准状况下,0.20L的容器中含某气体0.25g,求该气体的相对分子质量。
【思路点拨】标准状况下1mol气体的质量即为22.4L气体的质量。
【答案】28
【解析】气体密度为ρ==1.25g·L-1,气体的摩尔质量为1.25g·L-1×22.4L·mol-1=28g·mol-1,所以气体的式量为28。
【总结升华】求气体的式量即求气体的摩尔质量,若已知标准状况下气体密度为ρg·L-1,则气体的摩尔质量为M=22.4ρ。
举一反三:
【高清课堂:气体摩尔体积练一练1】
【变式1】在标准状况下,测得1.92g某气体的体积为672mL。计算此气体的相对分子质量。
【答案】64
【解析】该气体物质的量为:0.672L÷22.4 L·mol-1=0.03 mol,此气体的摩尔质量为1.92g÷0.03 mol=64 g·mol-1。故此气体的相对分子质量为64。
【变式2】标准状况下,89.6LCO和44.8LCO2混合,求混合气体的平均式量。
【答案】33.3
【解析】n(CO)= =4mol, n(CO2)= =2mol.
混合气体总物质的量n=4mol+2mol=6mol, 混合气体平均摩尔质量==33.3g·mol-1。
所以混合气体平均式量为33.3。
将上述求混合气体平均摩尔质量的计算式改变一下:
=28g·mol-1×+44g·mol-1×=33.3g·mol-1可见,求混合物的平均式量等于各组分的式量乘以物质的量分数或气体体积分数的加合。=M1x1+M2x2+.M1,M2……各组分的式量,x1, x2……各组分物质的量分数或气体体积分数。