- 322.00 KB
- 2024-03-27 发布
- 1、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 2、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报QQ:3215808601
2018-2019学年天津市静海县第一中学高一9月学生学业能力调研化学试题
考生注意:
1. 本试卷分第Ⅰ卷基础题(80分)和第Ⅱ卷提高题(20分)两部分,共100分。
2. 试卷书写规范工整,卷面整洁清楚,酌情减2-3分,并计入总分。
相对原子质量:H:1 C:12 N:14 O:16 S:32 Na:23 Cl:35.5
知识技能
学习能力
习惯养成
总分
内容
化学实验基本方法
物质的量
物质的分类和胶体
学法
卷面
整洁
分数
40
45
10
5
2-3
第Ⅰ卷 基础题(80分)
一、选择题: (每小题只有一个正确选项,共40分。)
1.滨海新区8.12爆炸事故给我们敲响了安全的警钟,对危险化学品要在包装上有警示标志。下列化学药品与其危险化学品图形标志不一致的一组是
A. 硫磺 B. 高锰酸钾 C. 氢气 D.乙醇
2.下列生产、生活、实验中的行为符合安全要求的是
A.进入煤矿井下作业,戴上安全帽,用帽上的矿灯照明
B.节日期间,可以在热闹繁华的商场里燃放烟花爆竹,欢庆节日
C.点燃打火机,可以检验液化气钢瓶口是否漏气
D.实验室里,可以将水倒入浓硫酸中及时用玻璃棒搅拌,配制稀硫酸
3.化学实验中必须注意安全,以下实验操作或事故处理中正确的是
①在点燃氢气、一氧化碳、甲烷等易燃气体前,必须检验气体的纯度
②做氢气还原氧化铜实验开始时,先通氢气后加热氧化铜
③浓碱液有腐蚀性,如不慎沾到皮肤上,应用较多的水冲洗,再涂上硼酸溶液
④给试管中的液体加热时,液体应不超过试管容积的
⑤点燃装满酒精的酒精灯
A.仅①②③④ B.仅①②③ C.仅①② D.①②③④⑤
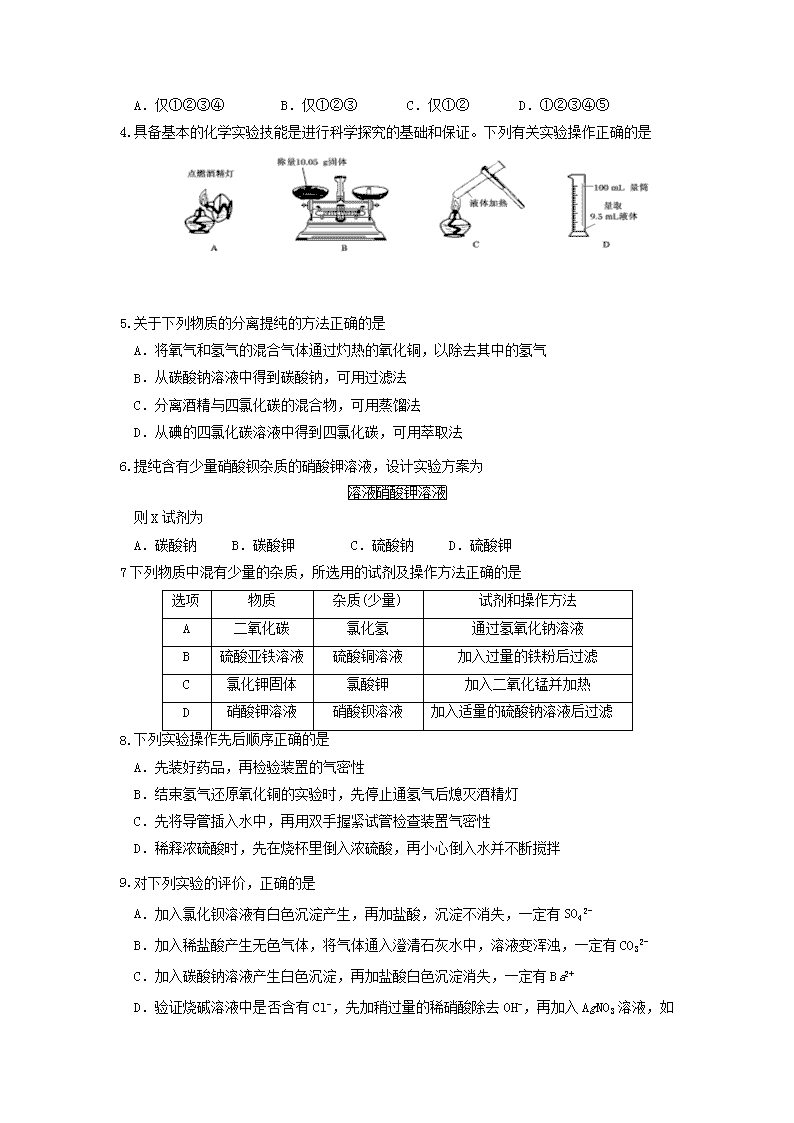
4.具备基本的化学实验技能是进行科学探究的基础和保证。下列有关实验操作正确的是
5.关于下列物质的分离提纯的方法正确的是
A.将氧气和氢气的混合气体通过灼热的氧化铜,以除去其中的氢气
B.从碳酸钠溶液中得到碳酸钠,可用过滤法
C.分离酒精与四氯化碳的混合物,可用蒸馏法
D.从碘的四氯化碳溶液中得到四氯化碳,可用萃取法
6.提纯含有少量硝酸钡杂质的硝酸钾溶液,设计实验方案为
则X试剂为
A.碳酸钠 B.碳酸钾 C.硫酸钠 D.硫酸钾
7下列物质中混有少量的杂质,所选用的试剂及操作方法正确的是
选项
物质
杂质(少量)
试剂和操作方法
A
二氧化碳
氯化氢
通过氢氧化钠溶液
B
硫酸亚铁溶液
硫酸铜溶液
加入过量的铁粉后过滤
C
氯化钾固体
氯酸钾
加入二氧化锰并加热
D
硝酸钾溶液
硝酸钡溶液
加入适量的硫酸钠溶液后过滤
8.下列实验操作先后顺序正确的是
A.先装好药品,再检验装置的气密性
B.结束氢气还原氧化铜的实验时,先停止通氢气后熄灭酒精灯
C.先将导管插入水中,再用双手握紧试管检查装置气密性
D.稀释浓硫酸时,先在烧杯里倒入浓硫酸,再小心倒入水并不断搅拌
9.对下列实验的评价,正确的是
A.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42-
B.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32-
C.加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
D.验证烧碱溶液中是否含有Cl-,先加稍过量的稀硝酸除去OH-,再加入AgNO3溶液,如有白色沉淀,则证明有Cl-
10.下列关于胶体的叙述,不正确的是
A.布朗运动是胶体微粒特有的运动方式,可以据此把胶体、溶液和悬浊液区别开来
B.光线透过胶体时,胶体发生丁达尔效应
C.用渗析的方法净化胶体时,使用的半透膜只能让较小的分子、离子通过
D.向氢氧化铁胶体中滴加硫酸溶液的现象是先形成沉淀后沉淀消失
11.下列叙述正确的是
A.摩尔是化学上常用的一个物理量
B.一个水分子的质量约等于 g
C.3.01×1023个SO2分子的质量约为16g
D.标准状况下,某物质含有6.02×1023个粒子,则该物质的体积为22.4L
12.NA表示阿伏加德罗常数的值,下列说法正确的是
A.1molCH中含有电子数为10NA
B.在标准状况下,11.2L氖气含有0.5NA个氖原子
C.物质的量浓度为0.5mol·L-1的MgCl2溶液中,含有Cl-数为NA
D.标准状况下,11.2L四氯化碳中含有的分子数为0.5NA
13.对于2 mol·L-1的BaCl2溶液,下列叙述正确的是( )
A.1 L溶液中约含2×6.02×1023个Cl-
B.取0.5 L该溶液,则c(Ba2+)为1 mol·L-1
C.0.5 L该溶液中Ba2+和Cl-总数约为3×6.02×1023个
D.取0.1 L溶液,则Cl-浓度为0.2 mol·L-1
14.下列溶液中溶质的物质的量浓度为1 mol/L的是
A.将40 g NaOH溶解在1 L水中
B.将22.4 L HCl气体溶于水配成1 L溶液
C.将1 L 10 mol/L浓盐酸加入9 L水中
D.将10 g NaOH溶解在水中配成250 mL溶液
15.下列关于物质的量浓度表述正确的是( )
A.0.3 mol·L-1的Na2SO4溶液中含有Na+和SO的总物质的量为0.9 mol
B.当1 L水吸收22.4 L氨气时所得氨水的浓度不是1 mol·L-1,只有当22.4 L氨气溶于水制得1 L氨水时,其浓度才是1 mol·L-1
C.在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO的物质的量相等,则K+和Cl-的物质的量浓度一定相等
D.10 ℃时,0.35 mol·L-1的KCl饱和溶液100 mL蒸发掉5 g水,冷却到10 ℃时,其体积小于100 mL,它的物质的量浓度仍为0.35 mol·L-1
16. 将36.5 g氯化氢溶解在1 L水中(水的密度近似为1 g·mL-1),所得溶液的密度为ρ g·mL-1,质量分数为w,物质的量浓度为cmol·L-1,NA表示阿伏加德罗常数的值,则下列叙述正确的是
A.所得溶液的物质的量浓度为1mol·L-1
B.36.5g氯化氢含有NA个原子
C.36.5gHCl气体占有的体积为22.4L
D.所得溶液的质量分数w=
17.某溶液中大量存在以下浓度的五种离子:0.4 mol/L Cl﹣、0.8 mol/L SO42﹣、0.2 mol/L Al3+、0.6 mol/L H+、和M离子,则M离子及其物质的量浓度可能为
A. Na+ 0.6mol/L B. CO32﹣ 0.2 mol/L C. Mg2+ 0.4 mol/L D. Ba2+ 0.4mol/L
18.已知质量分数为98%的浓硫酸(密度为1.84g·cm-3),其物质的量浓度为18.4mol/L,取10ml该硫酸与a mL水混合,配成质量分数为49%的硫酸(密度为1.40 g·cm-3),其物质的量浓度为b mol/L,则a、b分别为
A.a=10,b=9.2 B.a<10,b>9.2 C.a>10,b<9.2 D.a>10,b=9.2
19.已知Q与R的摩尔质量之比为9∶22,在反应X+2Y===2Q+R中,当1.6 g X与Y完全反应后,生成4.4 g R,则参与反应的Y和生成物Q的质量之比为
A.46∶9 B.32∶9 C.23∶9 D.16∶9
20.意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子,N4分子的结构如图所示,下列说法正确的是
A.N4属于一种新型的化合物
B.N4与N2的摩尔质量相等
C.等质量的N4与N2所含的原子个数比为1∶1
D.等质量的N4与N2所含的分子个数比为2∶1
二、填空题:(34分)
21.(6分)易混易错题组:将代表下列各分离物质方法的字母,填在相应的位置上。
A.萃取分液法 B.加热分解法 C.结晶法
D.分液法 E.蒸馏法 F.过滤法
(1)分离饱和食盐水与沙子的混合物________。
(2)从硝酸钾和氯化钠的混合溶液中获得硝酸钾________。
(3)分离水和汽油的混合物________。
(4)分离四氯化碳(沸点为76.6℃)和甲苯(沸点为110.6℃)的混合物________。
(5)从碘的水溶液里提取碘________。
(6)学法题:总结分离提纯方法选择的原则 (举例说明)
22.(11分)规律方法提炼题组:有关物质的量的计算
(1)在标准状况下,67.2LCO2是 mol,质量为 g,含有 个CO2分子,其中含有 mol氧原子。
(2)在标准状况下,1.7g氨气所占的体积约为 L,它与同条件下 mol H2S含有相同的氢原子数。
(3)某气态氧化物化学式为RO2,在标准状况下,1.28g该氧化物的体积是448mL,则氧化物的摩尔质量为_ __,R的相对原子质量为 。
(4)实验室常用浓硫酸的质量分数为98%,密度为1.80g·mL-1,其物质的量浓度是__ ___。(5)标准状况下,将V L A气体(摩尔质量为M g/mol)溶于0.1L水(密度1 g/cm3)中,所得溶液的密度为,则此溶液的物质的量浓度为 mol/L
A. B. C. D.
(6)学法题:通过以上训练思考,解决这些问题的关键是将其它量均先转化为
再计算。
三、化学实验题组(共23分)
23.粗盐提纯:粗盐中含有不溶性泥沙,可溶性的CaCl2、MgCl2、以及一些硫酸盐等。
(1)除去粗盐中的不溶性杂质,各步实验操作的名称依次为_________;________;_______。
(2)用上述方法提纯后的食盐中还含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:① 加入稍过量的Na2CO3溶液;② 加入稍过量的NaOH溶液;③ 加入稍过量的BaCl2 溶液;④滴入稀盐酸至无气泡产生;⑤ 过滤
正确的操作顺序是
A.②③①④⑤ B.①②③⑤④ C.③②①⑤④ D.③⑤②①④
24.蒸馏水的制取:如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题。
(1)A仪器的名称是________,B仪器的名称是________。
(2)实验时A中除加入少量自来水外,还需加入少量________,
其作用是___________。
(3)指出图中两处明显的错误,并改正:
①____________________;
②______________________。
(4)收集完蒸馏水后,是先撤酒精灯还是先关闭冷凝水?____________________________。
25.碘的提取:为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
已知步骤④中反应的化学方程式是Cl2+2KI===2KCl+I2。请填写下列空白:
(1)步骤③的实验操作名称是________。步骤⑥的实验操作名称是________。
(2)步骤⑤的操作名称是________,除烧杯外,还必须用到的玻璃仪器是________。
(3)从碘水溶液中提取碘,还可以选用下列__________(填字母)物质作为萃取剂。
a.酒精 b.苯(密度比水小) c.氯化钠溶液 d.醋酸
(4)以下关于萃取分液操作的叙述中,不正确的是______。
A.水溶液中加入乙醚,转移至分液漏斗中,塞上玻璃塞,如右图用力振荡
B.振荡几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振荡并放气后,手持分液漏斗静置待液体分层
D.分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗口上的小孔,再打开旋塞待下层液体全部流尽时,再从上口倒出上层液体
第Ⅱ卷 提高题(20分)
26.(1)下列仪器使用前必须检查是否漏水的有 (填序号)
A.容量瓶 B.蒸馏烧瓶 C.分液漏斗 D.量筒 E.蒸发皿
(2)实验室用Na2CO3·10H2O晶体配制0.5mol/L的Na2CO3溶液970mL,应选用的容量瓶的规格 ,称取Na2CO3·10H2O的质量是
(3)某学生欲用12mol·L-1浓盐酸和蒸馏水配制480mL物质的量浓度为0.3 mol·L-1的稀盐酸。
①该学生需要量取________mL上述浓盐酸进行配制。
②配制过程中正确的操作顺序是(字母表示,每个字母只能用一次)_____;
A. 用少量水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸,沿玻璃棒倒入烧杯中,再加入少量水,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL容量瓶中
D. 将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
③下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填 “偏大”、 “
偏小”、 “无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水
c.稀释浓盐酸时,未冷却到室温即转移到容量瓶中
d.将量取浓盐酸的量筒进行洗涤,并将洗涤液转移到容量瓶中
e.容量瓶洗涤干净后未干燥
(4)下图是某同学在实验室配制该NaCl溶液的过程示意图,其中有错误的是________(填操作序号)。
静海一中2018-2019第一学期高一化学(9月)
学生学业能力调研试卷答题纸
得分框
知识技能
学习能力
习惯养成
总分
第Ⅰ卷 基础题(共80分)
一、 选择题( 每小题2分,共40分。 每小题只有一个正确选项。)
题号
1
2
3
4
5
6
7
8
9
10
答案
题号
11
12
13
14
15
16
17
18
19
20
答案
二、填空题:(60分)
21.(12分)易混易错题组:
(1)________(2)________(3)________(4)________(5)________
(6)学法题:
22.(20分)规律方法提炼题组:
(1) , , , 。
(2) , 。
(3)_ __, 。
(4) (5)
(6)学法题:解决问题的关键是将其它量均先转化为 再计算。
三、化学实验题组
23.(1) ; ; _。(2)
24.(1)____ ____,_____ ___。
(2)_____ ___,_______ ____。
(3)①____________________ ;
②____________________ __。
(4)_____________ _________________。
25.(1)________ ,_______ _。
(2)_____ ___,____ ____。
(3)_____ _____(4)
第Ⅱ卷 提高题(20分)
26.(1) (2)
(3)①______ __ ②_
③a. b. c. d. e.
(4)
答案
1-5 CAACC 6-10 BBCDA
11-15 BBCDD 16-20 DCCDC
21.(1)F (2)C (3)D (4)E (5)A (6)略
22.(1)-(4)略 (5)B (6)略
23.(1)溶解 过滤 蒸发 (2)C
24.(1)蒸馏烧瓶 冷凝管 (2)碎瓷片或沸石 防止暴沸 (3)略
(4)先撤酒精灯后关闭冷凝水
25.(1)过滤 蒸馏 (2)萃取分液 分液漏斗 (3)b (4)ABC
26.(1)AC
(2)1000毫升容量瓶 93.0
(3)①12.5 ② BCAFED ③偏小 偏小 偏大 偏大 无影响
(4)①③⑤
您可能关注的文档
- 2018-2019学年天津市静海县第一中学高一9月学生学业能力调研化学试题
- 生物卷·2019届黑龙江省牡丹江市第一高级中学高二4月月考(2018-04)
- 2020参加巡察工作心得体会3篇
- 专题5-2 平面向量基本定理及坐标表示(练)-2018年高考数学(文)一轮复习讲练测
- 关于教师年度考核个人工作总结五篇
- 吉林省白城市洮南市第一中学2019-2020学年高二下学期第一次月考化学试题
- 2020年某社区党支部开展巡察整改专题组织生活会个人对照检查报告范文
- 辽宁省北票市高级中学高三政治一轮复习学案:唯物论
- 2020年下半年学校工会工作计划范文
- 2017-2018学年湖北省襄阳市四校(襄州一中、枣阳一中、宜城一中、曾都一中)高二上学期期中联考英语试题